
 工业尾气SO2有多种吸收和处理方法.
工业尾气SO2有多种吸收和处理方法.分析 (1)Na2SO3溶液吸收SO2生成NaHSO3;
(2)①Pt(1)电极进入SO2,硫酸浓度增大,SO2可知失电子,作负极,电极上二氧化硫被氧化生成硫酸;
②左侧电极反应式为:SO2-2e-+2H2O=SO42-+4 H+,根据电子转移守恒计算生成硫酸根、氢离子的物质的量,为保持溶液电中性,多余的氢离子通过阳离子交换膜移至右侧,左侧溶液中增加离子为生成硫酸电离的离子总量;
(3)甲酸钠和氢氧化钠混合溶液与SO2生成保险粉同时生成二氧化碳,依据反应物和生成物结合原子守恒、电荷守恒配平写出.
解答 解:(1)Na2SO3溶液吸收SO2的离子方程式为SO32-+SO2+H2O=2HSO3-,故答案为:SO32-+SO2+H2O=2HSO3-;
(2)①由图可知,Pt(1)电极上二氧化硫被氧化生成硫酸,电极反应式为:SO2-2e-+2H2O=SO42-+4 H+,
故答案为:SO2-2e-+2H2O=SO42-+4H+;
②左侧电极反应式为:SO2-2e-+2H2O=SO42-+4H+,根据电子转移守恒,生成硫酸根物质的量$\frac{0.02mol}{2}$=0.01mol,生成氢离子为0.04mol,为保持溶液电中性,0.01mol硫酸根需要0.02mol氢离子,多余的氢离子通过阳离子交换膜移至右侧,即有0.02mol氢离子移至右侧,故左侧溶液中增加离子为0.01mol+0.02mol=0.03mol,
故答案为:0.03;
(3)甲酸钠和氢氧化钠混合溶液与SO2生成保险粉Na2S2O4同时生成二氧化碳,反应的离子方程式:HCOO-+OH-+2SO2═S2O42-+H2O+CO2
故答案为:HCOO-+OH-+2SO2═S2O42-+H2O+CO2.
点评 本题涉及电极反应式书写、电解池有关计算等,需要学生具备扎实的基础,侧重考查学生对知识的迁移应用,(2)中左侧溶液中增加离子物质的量计算为易错点,学生容易根据电极反应式计算,忽略部分氢离子移至右侧.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| 实验序号 | 1 | 2 | 3 |
| V(盐酸)/mL | 50 | 50 | 50 |
| m(混合物)/g | 9.2 | 15.7 | 27.6 |
| V(CO2)(标准状况)/L | 2.24 | 3.36 | 3.36 |
| A. | 实验②中,混合物过量 | |
| B. | 原混合物样品中n(NaHCO3):n(KHCO3)=1:1 | |
| C. | 盐酸的物质的量浓度为2mol•L-1 | |
| D. | 实验反应后,至少需继续加入50mL的盐酸溶液才能使27.6g的混合物全部反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| C. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏 | |
| D. | 除去甲烷中混有的少量乙烯:将混合气体通入酸性KMnO4溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
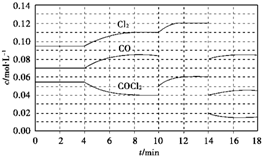
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第I A族元素的化合物 | B. | 第III A族元素的化合物 | ||
| C. | 第IV A族元素的化合物 | D. | 第VII A族元素的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| C. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L | |
| B. | V L Fe2(SO4)3溶液中含a g SO42-,取此溶液0.5VL用水稀释成2V L,则稀释后溶液的c(Fe3+)为$\frac{a}{4V}$ mol/L | |
| C. | 实验室需240mL2mol/L的CuSO4溶液,配置时应称125.0gCuSO4•5H2O | |
| D. | 10mL质量分数为98%的H2SO4,用水稀释至100mL,质量分数变为9.8% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com