
(1)实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。理论上硫酸和硝酸的物质的量之比最佳为:_________________________________。
(2)实际上,即使铜粉、硫酸及硝酸都比较纯,制得的CuSO4·5H2O中还是有可能存在的杂质是________,除去这种杂质的实验操作称为_____________________________。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案甲:以空气为氧化剂。将铜粉在________(填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案乙:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5 mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
请回答下列问题:已知:Ksp[Cu(OH)2]≈10-22,Ksp[Fe(OH)2]≈10-16,Ksp[Fe(OH)3]≈10-38
①为了使铁元素全部沉淀,应调节pH至少为______________________________;
②甲物质可选用的是________;
A.CuCl2 B.NaOH C.Cu2(OH)2CO3 D.CuO E.H2SO4
③反应中加入少量FeSO4对铜的氧化可以起催化作用。其反应过程是:第1步,4Fe2++O2+4H+===4Fe3++2H2O,请写出其第2歩反应的离子方程式_____________________
________________________________________________________________________。
方案丙:将铜丝放到一定量的稀硫酸中,加入适量的H2O2,并控温在50 ℃~60 ℃,持续反应1 h,也能获得硫酸铜。请回答下列问题:
④反应时温度必须控制在50 ℃~60 ℃,温度不宜过高的主要原因是________________________________________________________________________;
⑤写出该反应的化学方程式为__________________________________________。
解析 (1)据3Cu+8H++2NO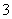 =
= ==2NO↑+4H2O+3Cu2+,硝酸提供2H+,而硫酸提供6H+,故理论上硫酸和硝酸的物质的量之比最佳为3∶2。
==2NO↑+4H2O+3Cu2+,硝酸提供2H+,而硫酸提供6H+,故理论上硫酸和硝酸的物质的量之比最佳为3∶2。
(2)制得的CuSO4·5H2O中还是有可能存在的杂质是Cu(NO3)2,分离CuSO4和Cu(NO3)2,利用溶解度 上的差异进行重结晶。
上的差异进行重结晶。
(3)灼烧固体要用的仪器就是坩埚,①已知:Ksp[Cu(OH)2]≈10-22,Ksp[Fe(OH)2]≈10-16,Ksp[Fe(OH)3]≈10-38应该加入能够与H+反应的物质调节pH值,让铁元素以Fe(OH)3形式析出来;Ksp[Fe(OH)3]≈10-38=10-5×c(OH-)3,可以求出c(OH-)=10-11,求出pH=3,又不引入杂质离子又能与H+反应调节pH值,可选用Cu2(OH)2CO3或者CuO。③2Fe3++Cu===2Fe2++Cu2+。④反应时温度必须控制在50 ℃~60 ℃,温度不宜过高的主要原因是防止双氧水分解。⑤Cu+H2O2+H2SO4===CuSO4+2H2O。
答案 (1)3∶2 (2)Cu(NO3)2 重结晶 (3)坩埚 ①3 ②CD ③2Fe3++Cu===2Fe2++Cu2+ ④防止双氧水分解 ⑤Cu+H2O2+H2SO4===CuSO4+2H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
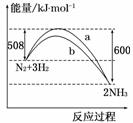 如图,a曲线是198 K、101 k
如图,a曲线是198 K、101 k Pa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
Pa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
A.该反应的热化学方程式为:
N2+3H2 2NH3
2NH3
ΔH=-92 kJ·mol-1
B.b曲线是升高温度时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在198 K、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ则184>Q2>2Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
具有单双键交替长链(如:
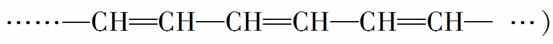 的高分子化合物有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是( )
的高分子化合物有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3位科学家。下列高分子中可能成为导电塑料的是( )
A.聚乙烯 B.聚丁二烯
C.聚苯乙烯 D.聚乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
要组装一套实验室利用液体和液体反应制备气体的装置,现设计了如下的五步操作 ,正确的程序是
,正确的程序是
①将蒸馏烧瓶固定在铁架台上 ②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网 ③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集装置中 ④检查装置的气密性(利用固定装置微热的方法检查气密性) ⑤在蒸馏烧瓶中装好分液漏斗,连接好导气管
A.②①⑤④③ B.④①②⑤③
C.①②⑤④③ D.①⑤④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
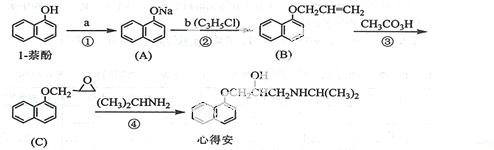
回答下列问题:
(1)试剂a是__________,试剂b的结构简式为________,b中官能团的名称是____________。
(2)③的反应类型是______________。
(3)心得安的分子式为______________。
(4)试剂b可由丙烷经三步反应合成:
C3H8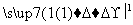 X
X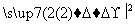 Y
Y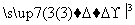 试剂b
试剂b
反应1的试剂与条件为____________,反应2的化学方程式为____________________________________________,反应3的反应类型是__________。(其他合理答案也可)
(5)芳香化合物D是1萘(酚)的同分异构体,其分子中有两个官能团,能发生银镜反应,D能被KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,F芳环上的一硝化产物只有一种。D的结构简式为____________________;
由F生成一硝化产物的化学方程式为________________________________________________________________,该产物的名称是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
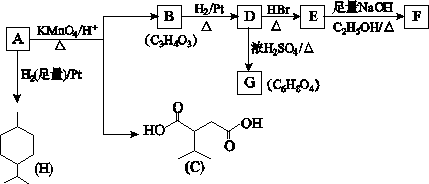
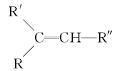
从薄荷油中得到一种烃A(C10H16),叫α非兰烃,与A相关反应如下:
 | |||
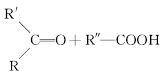 | |||
已知: 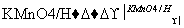
(1)H的分子式为____________。
(2)B所含官能团的名称为____________。
(3)含两个—COOCH3基团的C的同分异构体共有________种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体的结构简式为______________。
(4)B→D,D→E的反应类型分别为______________、____________。
(5)G为含六元环的化合物,写出其结构简式:______________。
(6)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂名称为___________。
(7)写出E→F的化学反应方程式:_________________________。
(8)A的结构简式为____________,A与等物质的量的Br2进行加成反应的产物共有________种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质水解的说法正确的是( )
A.蛋白质水解的最终产物是多肽
B.淀粉水解的最终产物是葡萄糖
C.纤维素不能水解成葡萄糖
D.油脂水解产物之一是甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于

①2∶7 ②5∶4 ③4∶5 ④7∶2
A.①② B.②④
C.③④ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com