
【题目】在恒温恒容的密闭容器中可逆反应2NO2(g)![]() 2NO(g)+O2(g),达到平衡状态的标志是
2NO(g)+O2(g),达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO2
②单位时间内生成n molO2的同时生成2n mol NO
③混合气体的颜色不再改变的状态
④用NO2、NO、O2表示的反应速率的比为2:2:1的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
⑧2V正(NO2)=2V逆(O2)
A.①③⑥⑦ B.②⑤⑥⑦ C.①③④⑤⑧ D.①②③④⑤⑥⑦⑧
【答案】A
【解析】
试题分析:①单位时间内生成nmolO2是正反应速率,同时生成2nmolNO2是逆反应速率,且化学反应速率之比等于化学计量数之比,故正逆反应速率相等,说明达到平衡状态,①正确;②单位时间内生成nmolO2是正反应速率,同时生成2nmolNO也是正反应速率,故不能说明达到平衡状态,②错误;③二氧化氮为红棕色气体,一氧化氮和氧气为无色气体,故混合气体的颜色不再改变,说明达到平衡状态,③正确;④化学反应速率之比等于化学计量数之比,故用NO2、NO、O2的物质的量浓度变化表示的反应速率的比始终为2:2:1,故不能说明达到平衡状态,④错误;⑤密度=![]() ,总质量不变,体积不变,故混合气体的密度不再改变,不能说明达到平衡状态,⑤错误;⑥反应前后气体的物质的量不等,故混合气体的压强不再改变,说明达到平衡状态,⑥正确;⑦平均相对分子质量=
,总质量不变,体积不变,故混合气体的密度不再改变,不能说明达到平衡状态,⑤错误;⑥反应前后气体的物质的量不等,故混合气体的压强不再改变,说明达到平衡状态,⑥正确;⑦平均相对分子质量=![]() ,总质量不变,总物质的量会变,故混合气体的平均相对分子质量不再改变,说明达到平衡状态,⑦正确;达到平衡状态的标志是①③⑥⑦,答案选A。
,总质量不变,总物质的量会变,故混合气体的平均相对分子质量不再改变,说明达到平衡状态,⑦正确;达到平衡状态的标志是①③⑥⑦,答案选A。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中充入一定量SO2、O2发生反应2SO2(g)+O2(g)![]() 2SO3(g), 测得SO3浓度与反应温度关系如图.下列说法正确的是
2SO3(g), 测得SO3浓度与反应温度关系如图.下列说法正确的是
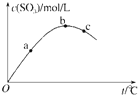
A.该反应△H>0
B.SO2转化率:a>b>c
C.化学反应速率:c>b>a
D.平衡常数K:b>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、T是原子序数依次増大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族。T的单质常用于自来水的杀菌消毒。
请回答下列问题:
(1)W元素在周期表中的位置为:____________________
(2)由 X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为____________________。
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:______________
(4)Y和T两元素的非金属性强弱为Y________T (填“>”“<”或者“=”)。可以验证该结论的方法是___________________
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(5)某化学兴趣小组欲通过实验探究元素N、C、Si 非金属性强弱。实验装置如下:
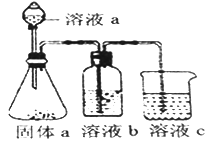
①溶液a和溶液b分别为__________溶液、________溶液(填溶质化学式)
②经验证,N、C、Si的非金属性由强到弱为:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,成为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为__________,D的化学名称为__________。
(2)①和③的反应类型分别为__________、__________。
(3)E的结构简式为__________。用1 mol E合成1,4—二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2—苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝的叙述中,不正确的是( )
A.铝是地壳里含量最多的金属元素
B.铝容易失去电子,表现还原性
C.在空气中用酒精灯点不着
D.在常温下,铝不能与氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化
C.实验室中常用排饱和食盐水的方法收集Cl2
D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量分数为10%NaOH溶液,加热蒸发掉100g水后得到80mL质量分数为20%的溶液,则该质量分数为20%NaOH溶液的物质的量浓度为
A.6.25mol·L-1
B.12.5mol·L-1
C.7mol·L-1
D.7.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把23g钠投入到m1g足量的水中得到ag溶液,把24g镁投入到m2g足量的盐酸中得到bg溶液,若m1=m2 , 则a , b的关系是( )
A.a>b
B.a<b
C.a=b
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g),达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
SO3(g)+NO(g),达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是

A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2时,SO2的转化率:a~b段小于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com