
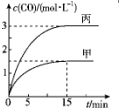
 一定条件下存在反应C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、丙两个恒容容器中加入一定量C和H2O(g),向乙恒容容器中加入一定量CO和H2,各容器中温度、反应物的起始量如表,甲、丙反应过程中CO的物质的量浓度随时间变化如图.
一定条件下存在反应C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、丙两个恒容容器中加入一定量C和H2O(g),向乙恒容容器中加入一定量CO和H2,各容器中温度、反应物的起始量如表,甲、丙反应过程中CO的物质的量浓度随时间变化如图.| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2mol C、 1mol H2O(g) | 1mol CO、 1mol H2 | 4mol C、 2mol H2O(g) |
| A. | 丙容器的容积V<0.5L | |
| B. | 甲容器中,反应在前15 min内的平均反应速率v(H2)=0.15 mol•L-1•min-1 | |
| C. | 当温度为T1℃时,反应的平衡常数K=2.25 | |
| D. | 乙容器中,若平衡时n(H2O)=0.3 mol,则T1<T2 |
分析 A、丙容器中起始量为甲的二倍,若容积=0.5 L,由于正反应为气体体积增大的反应,加压平衡左移,c(CO)<3mol/L;
B、由图可知,15min内甲容器中CO的浓度变化量为1.5mol/L,根据v=$\frac{△c}{△t}$计算v(CO),再利用速率之比等于化学计量数之比计算v(H2);
C、根据甲容器中反应数据计算 T1℃时各物质的平衡浓度,再根据平衡常数K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$计算;
D、比较甲与乙可知,二者达等效平衡,根据甲、乙容器中平衡时n(H2O)的量可知,乙相对于甲平衡向逆反应移动,因为正反应吸热,乙中温度低,即温度T1>T2.
解答 解:A、丙容器中起始量为甲的二倍,若容积=0.5 L,由于正反应为气体体积增大的反应,加压平衡左移,c(CO)<3mol/L,故丙容器的体积V<0.5 L,故A正确;
B、由图可知,15min内甲容器中CO的浓度变化量为1.5mol/L,v(CO)=$\frac{1.5mol/L}{15min}$=0.1mol•L-1•min-1,速率之比等于化学计量数之比,所以v(H2)=0.1mol•L-1•min-1,故B错误;
C、根据甲容器中反应数据计算:
C(s)+H2O(g)═CO(g)+H2(g)
起始浓度(mol/L) 2 0 0
转化浓度(mol/L) 1.5 1.5 1.5
平衡浓度(mol/L) 0.5 1.5 1.5
T1℃时,反应的平衡常数K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$=$\frac{1.5×1.5}{0.5}$=4.5,故C错误;
D、比较甲与乙可知,二者达平衡是等效的,经计算知甲容器中平衡时n(H2O)=0.25 mol,乙容器中,若平衡时n(H2O)=0.4 mol,乙相对于甲平衡向逆反应移动,因为正反应吸热,乙中温度低,即温度T1>T2,故D错误;
故选A.
点评 本题考查化学平衡移动、计算及化学平衡图象,题目难度中等,注意理解图象的纵坐标和横坐标的意义.


科目:高中化学 来源: 题型:选择题
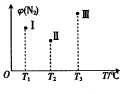 分别在Tl℃、T2℃、T3℃时,向三个500mL 的恒容密闭容器中均充人1molN2和2.5molH2,发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.实验测得反应tmin 时N2的体积分数如图所示.下列说法正确的是( )
分别在Tl℃、T2℃、T3℃时,向三个500mL 的恒容密闭容器中均充人1molN2和2.5molH2,发生反应:N2(g)+3H2(g)?2NH3(g)△H<0.实验测得反应tmin 时N2的体积分数如图所示.下列说法正确的是( )| A. | 在t min时,Ⅱ和Ⅲ一定达平衡状态 | |
| B. | 2v(NH3)=3v(H2)时,三个容器均达平衡状态 | |
| C. | 平衡后容器Ⅰ中混合气体的平均相对分子质量最小 | |
| D. | 已知tmin时,Ⅲ中c(N2)=1mol/L,此时反应平衡常数K=0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
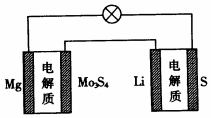 已知:镁电池的总反应为xMg+Mo3S4$?_{放电}^{充电}$MgxMo3S4,锂硫电池的总反应为2Li+S$?_{放电}^{充电}$Li2S.下列说法正确的是( )
已知:镁电池的总反应为xMg+Mo3S4$?_{放电}^{充电}$MgxMo3S4,锂硫电池的总反应为2Li+S$?_{放电}^{充电}$Li2S.下列说法正确的是( )| A. | 镁电池放电时,Mg2+向负极迁移 | |
| B. | 镁电池放电时,正极发生的电极反应为Mo3S4+2xe-=Mo3S42- | |
| C. | 理论上两种电池的比能量相同(参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量) | |
| D. | 图中Li作负极,Mo3S4作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B. | C. | D. |
| 《神农本草经》记载,麻黄能“止咳逆上气” | 胃舒平药片 (复方氢氧化铝)  |  |  秦朝彩俑 |
| 古代中国人已用麻黄治疗咳嗽 | 该药是抗酸药,服用时喝些醋能提高药效 | 看到有该标志的丢弃物,应远离并报警 | 古代中国人掌握化学制颜料方法 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | NaHCO3能与碱反应,可用作焙制糕点的膨松剂 | |
| C. | 浓硫酸具有脱水性,可用于干燥氢气 | |
| D. | MgO、Al2O3熔点高,可用于制作耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 棉花和蚕丝的主要成分都是纤维素 | |
| B. | 蛋白质在一定条件下发生水解反应生成葡萄糖 | |
| C. | 煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程 | |
| D. | 合成材料的大量使用给人类带来了严重污染,所以要禁止生产和使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 铝箔在空气中受热可以融化,由于氧化膜的存在,融化的铝并不滴落 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纳米材料是指一种称为“纳米”的新物质制成的材料 | |
| B. | 复合材料一般有强度高、质量轻、耐高温、耐腐蚀等优异性能,其综合性质超过了单一材料 | |
| C. | 淀粉和纤维素通式都是(C6H10O5)n,都是天然高分子化合物 | |
| D. | 合成纤维的主要原料是石油、天然气、煤等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com