
���� ��1������c=$\frac{1000�Ѧ�}{M}$����25%����������ʵ���Ũ�ȣ�����ҪŨ��������ΪV������ϡ��ǰ����Һ���������ʵ����ʵ��������������Ũ��������V��
��2������������Һ�����ѡ����ʵ�����ƿ��
��3��B��������Һ�������������ʵ������ڢ٢�����������Һ��������ܵ����ʵ����Ӣ��ṩ��������ʵ��������Ԣ��ṩ��������ʵ����������������ܵ����ʵ�����ȥ�٢�����������Һ��������ܵ����ʵ���������V=$\frac{n}{c}$���������
D���ձ��ںͲ������϶�մ�����ᣬΪ��֤ȫ��������ת�Ƶ�����ƿ��Ӧ����ϴ�ӣ���ϴ��Һȫ��ת�Ƶ�����ƿ�У�
��4������c=$\frac{n}{V}$������D������n��Ӱ�죻
��5������ƿΪ�����������������ܽ����ϡ�ͻ�ų��������ȣ�
��� �⣺��1��25%����������ʵ���Ũ��Ϊ��c=$\frac{1000��1.18��25%}{98}$=3.0mol/L��
�ʴ�Ϊ��3.0��
��2��������ijѧ��������6.0mol/L��H2SO4 1000mL��Ӧѡ��1000mL������ƿ��
�ʴ�Ϊ��1000��
��3��������6.0mol/L��H2SO4 1000mL������������ʵ���=6.0mol/L��1L=6.0mol����480mL 0.5mol/L�������к���������ʵ���Ϊ0.5mol/L��0.48L=0.24mol����150mL 25%�����ᣨ��=1.18g/mL������������ʵ���Ϊ3.0mol/L��0.15L=0.45mol��6.0mol-0.24mol-0.45mol=5.31mol��������Ҫ18mol/L����������V=$\frac{n}{c}$=$\frac{5.31mol}{18mol/L}$=0.2950L=295.0mL��
�ʴ�Ϊ��295.0��
D���ձ��Ͳ���������ȷ��ʵ������ǣ���������ˮϴ���ձ��Ͳ�����2��3�Σ�ϴ��Һ��ע������ƿ�У�
�ʴ�Ϊ����������ˮϴ���ձ��Ͳ�����2��3�Σ�ϴ��Һ��ע������ƿ�У�
��4������c=$\frac{n}{V}$�����ʡ�Բ���D�������ʵ����ʵ���n����ƫС��������Һ��Ũ�Ƚ���ƫС��
�ʴ�Ϊ��ƫС��
��5�������ڳ�����������Һ��Ӧ�ý�ϡ�ͺ��������ȴ�����£�
�ʴ�Ϊ����ϡ�ͺ��������ȴ�����£�
���� ���⿼����ҺŨ�ȵļ����һ�����ʵ���Ũ����Һ�����Ʒ�������Ŀ�Ѷ��еȣ�����ע��������Һ�IJ������衢�����Լ�ע���������ѧ����Ҫ�Ķ���ʵ�飬����������ѧ���ķ�����������ѧʵ��������


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10 mL0.1 mol•L-1��ˮ��10 mL0.1 mol•L-1�����ϣ�c��Cl-����c��NH4+����c��OH-����c��H+�� | |
| B�� | 10 mL0.1 mol•L-1NH4Cl��Һ��5 mL0.2 mol•L-1NaOH��Һ��ϣ�c��Na+��=c��Cl-����c��OH-����c��H+�� | |
| C�� | 10 mL0.1 mol•L-1CH3COOH��Һ��5 mL0.2 mol•L-1NaOH��Һ��ϣ�c��Na+��=c��CH3COO-����c��OH-����c��H+�� | |
| D�� | 10 mL0.5 mol•L-1CH3COONa��Һ��6 mL 1 mol•L-1�����ϣ�c��Cl-����c��Na+����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������84����Һ���ʹ�ã��ܸ���Ч����߳����������������� | |
| B�� | ���������������������ȡ�������ȡ�ű���ô�95%��100%��������ȡԭ���������������������� | |
| C�� | ʹ������ø���������ˮ�е��л���ɷ�ֹˮ��ĸ�Ӫ���� | |
| D�� | ������ά���ϳ����ά�������л��߷��ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ�Fe��OH��3���壺Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3H+ | |
| B�� | �Ҵ��Ľṹ��ʽ��C2H6O | |
| C�� | CO2�ı���ģ�ͣ� | |
| D�� | ������Ϊ8��������Ϊ17��ԭ�ӣ�${\;}_{8}^{17}$Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
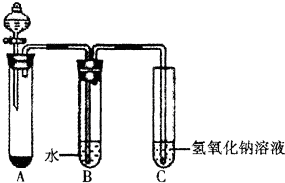 ij����С��ͬѧ����ͼ��ʾװ�ý���C12���Ʊ����������ʵ�飨���ȼ��г�װ����ʡ�ԣ���
ij����С��ͬѧ����ͼ��ʾװ�ý���C12���Ʊ����������ʵ�飨���ȼ��г�װ����ʡ�ԣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 02����������PtF6�ǻ�ԭ�� | |
| B�� | 02 ��PtF6������Ԫ�صĻ��ϼ�Ϊ+1 | |
| C�� | 02�� PtF6���в����ڹ��ۼ� | |
| D�� | ÿ����1 mol O2 ��PtF6����ת��1 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʴ���ǽ���ԭ��ʧȥ���ӱ������Ĺ��� | |
| B�� | ����������ʴʱ��������ӦʽΪ��2H20+O2+4e-�T4OH- | |
| C�� | ���ִ�����Ƕп���Ա������壬���õ����������������� | |
| D�� | �����������ڿ�������绯ѧ��ʴ�����䰵 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �� | C�� | ���� | D�� | ̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� | 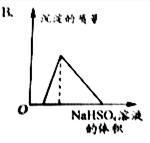 | ||
| C�� |  | D�� | 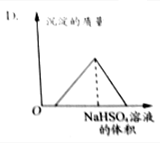 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com