
【题目】氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且使平衡混合物中NH3的体积分数一定增大的是______。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下向100m10.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
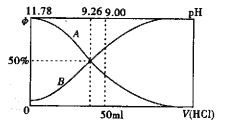
①表示NH3·H2O浓度变化的曲线是______(填“A”或“B")。
②NH3·H2O的电离常数为_______(已知1g1.8=0.26)
③当加入盐酸体积为50ml时,溶液中c(NH4+)-c(NH3·H2O)=____mol/L(用精确值表示)。
II.已知常温下,Ksp[Al(OH)3]=4.0×10-38,在AlCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:________________;若将所得悬浊液的pH调整为3,则溶液中Al3+浓度为_____mol/L。
【答案】 B A 1.8×10-5或10-4.74 10-5-10-9 Al3++3HCO3-=Al (OH)3↓+3CO2↑ 4.0×10-5
【解析】本题主要考查有溶液中的离子平衡。
I.(1)A.正反应速率减小,故A不符合题意;B. 正反应速率增大,且平衡右移使平衡混合物中NH3的体积分数,故B符合题意;C. 平衡混合物中NH3的体积分数减小,故C不符合题意;D. 平衡混合物中NH3的体积分数减小,故D不符合题意。故选B。
(2)①反应过程中氨水的pH减小,所以表示NH3·H2O浓度变化的曲线是A。
②NH3·H2O的电离常数为Kb=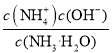 =
=![]() =1.8×10-5。
=1.8×10-5。
③当加入盐酸体积为50ml时,中和反应恰好完全进行,形成氯化铵溶液,溶液中 c(H+)=c(OH-)+c(NH3·H2O),所以c(NH4+)-c(NH3·H2O)= c(H+)-c(OH-)=(2×10-5-2×10-9)mol/L。
II.在AlCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为Al3++3HCO3-=Al (OH)3↓+3CO2↑;若将所得悬浊液的pH调整为3,c(OH-) =![]() =
=![]() mol/L=1×10-2mol/L,则溶液中Al3+浓度为
mol/L=1×10-2mol/L,则溶液中Al3+浓度为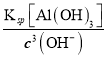 =4.0×10-5mol/L。
=4.0×10-5mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3·H2O) =1.76×10-5,下列说法正确的是
A. 常温下将pH=3的 HCOOH溶液和pH=11氨水等体积混合后溶液呈碱性
B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C. 0.2 mol·L-1 HCOOH 与 0.1 mol·L-1 NaOH 等体积混合后的溶液中:c(HCOO-) + c(OH-) = c(HCOOH) + c(H+)
D. 0.2 mol·L-1 CH3COONa 与 0.1 mol·L-1盐酸等体积混合后的溶液中(pH<7):c(CH3COOH) > c(Cl- ) > c(CH3COO-) > c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油裂解产物A可合成多种产物(如F是一种称为富马酸二甲酯的杀菌剂),下图用A合成一些有机产物的转化关系:
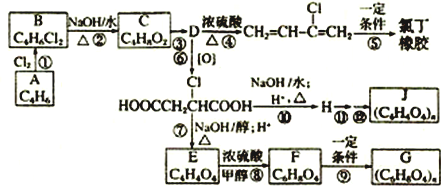
(1)上述反应中属于加成反应的是___________。(填序号)
(2)1H核磁共振谱图表明A分子只有两种化学环境不同的氢原子,红外光谱研究表明A分子中含有两个碳碳双键,请写出D的结构简式: _____________ 。
(3)写出B转化为C的化学方程式__________________________________________。
(4)H物质在浓硫酸存在下可分别生成一种含六元环、七元环、八元环的产物,写出生成六元环产物的化学方程式______________________________________。
(5)写出与A互为同分异构体,且分子中有4个碳原子共直线的有机物的结构简式: ____________。
(6)认真观察合成路线C→E,回答下列两个问题:
a.从C 到E,用了③⑥⑦三步反应,而不是一步进行,这样做的原因是______________。
b.被氧化成HOOC—CH2CHClCOOH的过程中会有中间产物生成,检验该中间产物的试剂是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室可用如图所示装置制取少量乙酸乙酯。有关叙述不正确的是( )

A. 长导管起冷凝、导气的作用
B. 用蒸馏法从所得混合溶液中分离出乙酸乙酯
C. Na2CO3饱和溶液的作用之一是吸收未反应的乙酸
D. 导管末端不插入饱和Na2CO3溶液中是为了防倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科研人员设计一种电化学反应器以Na2SO4溶液为电解质,负载纳米MnO2的导电微孔钛膜和不锈钢为电极材料。这种电催化膜反应器可用于正丙醇合成丙酸,装置示意图:

以下叙述错误的是
A. 微孔钛膜作阴极
B. 使用Na2SO4溶液是为了在电解开始时增强溶液导电性
C. 丙醇转化为丙酸的电极反应式为:CH3CH3CH2OH+H2O-4e-=CH3CH2COOH+4H+
D. 反应器工作时料槽中正丙醇分子向电催化膜移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入Fe2(SO4)3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等.则已经反应的Fe3+和未反应的Fe3+物质的量之比为( )
A.2:3
B.3:2
C.1:2
D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.其他条件不变时增大压强,能使全气体反应体系中活化分子百分数增加
B.中和反应都是放热反应
C.在FeCl3溶液和KSCN溶液反应的平衡体系中,加入KCl固体,平衡逆向移动
D.熵增大的反应不一定自发,但自发反应熵一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知浓度均为0.1 mol/L的8种溶液:①CH3COONa、②KCl、③NH4Cl 、④NaOH 、⑤Ba(OH)2、⑥HNO3、⑦H2SO4、⑧CH3COOH,其溶液的pH由小到大的顺序是__________________________(填写序号)。
(2)25℃时,若体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液混合,恰好中和。请回答:
若a+b=12,则Va: Vb=________。
若Va<Vb和a=0.5b,则a的取值范围是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用NaOH溶液滴定H2C2O4 溶液,溶液中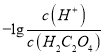 和-lgc(HC2O4-)或
和-lgc(HC2O4-)或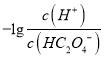 和-lgc(C2O42-)关系如图所示,下列说法正确的是
和-lgc(C2O42-)关系如图所示,下列说法正确的是
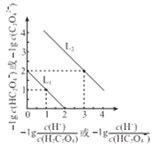
A. 曲线L1表示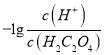 和-lgc(HC2O4-)的关系
和-lgc(HC2O4-)的关系
B. Ka2(H2C2O4)的数量级为10-2
C. NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 向0.1mol/LH2C2O4溶液中加入少量水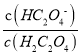 减小
减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com