
���� ��1��NO��ת�������¶����߶����ͣ�˵���÷�ӦΪ���ȷ�Ӧ�����¶Ⱥ�ƽ�����������ƶ�����Ӧ���ʼ�С���������������ƽ�ⳣ��������
��2��������������ˮ������ʳ��ˮ����ͨ�백����ͨ�������̼������̼�����ƾ��壻
��3��̼����������Һ�д��ڵ���ƽ��NaHCO3?HCO3-+Na+����������ʱ�ٽ���HCO3-��ˮ�⣻�������ʱ�ٽ���HCO3-�ĵ��룻
��4��H2CO3Ϊ��Ԫ���ᣬ���ȶ����Ե�һ������Ϊ������Һ��c��CO32-����С��
Na2CO3����Һ�е����̼������ӣ�̼������ӵ�ˮ��̶Ƚ�С������Һ��c��CO32-�����
NaHCO3����Һ�У�̼��������ӵ�ˮ��̶ȴ��������̶ȣ���Һ��Һ��̼�������Ũ�Ƚ�С��
NH4HCO3��Һ�У�笠�����ˮ����Һ�����ԣ�������̼��������ӵĵ��룬�ݴ˽��н��
��� �⣺��1����ӦC��s��+2NO��g��?N2��g��+CO2��g���У�NO��ת�������¶����߶����ͣ�˵�������¶�ƽ�����������ƶ�����÷�ӦΪ���ȷ�Ӧ���������¶ȣ����淴Ӧ���ʶ���С��ƽ���������ȵ�����Ӧ���У����������ʵ���������N2����������������ڽ����¶Ⱥ����Ͷ�����̼��Ũ������NO��Ũ�ȼ�С����ƽ�ⳣ����С��
�ʴ�Ϊ����С����������
��2���������Ͷ�����̼�Ⱥ�ͨ�뱥��ʳ��ˮ�з�����Ӧ��NH3+CO2+NaCl+H2O=NaHCO3��+NH4Cl������Һ�л��а�ɫ�������ɣ�
�ʴ�Ϊ����Һ���а�ɫ�������ɣ�NH3+CO2+NaCl+H2O=NaHCO3��+NH4Cl��
��3��̼����������Һ�д��ڵ���ƽ�⣺NaHCO3?HCO3-+Na+����NaHCO3��Һ������ʱ���ٽ���HCO3-��ˮ�⣬����CO2���������ʱ���ٽ���HCO3-�ĵ��룬����̼�����Σ�
�ʴ�Ϊ����NaHCO3��Һ������ʱ���ٽ���HCO3-��ˮ�⣬����CO2���������ʱ���ٽ���HCO3-�ĵ��룬����̼�����Σ�
��4���ۢ���Ƚϣ�����笠�����ˮ������ԣ�������̼��������ӵĵ��룬c��CO32-����СΪ���ۣ��ܣ���Ϊ��Ԫ���ᣬc��CO32-����С����Na2CO3����Һ�е���������Ӻ�̼������ӣ�̼�������ˮ��̶Ƚ�С��������Һ��c��CO32-���������c��CO32-���Ĵ�С��ϵΪ��Na2CO3��NaHCO3��NH4HCO3��H2CO3�������ڣ��ۣ��ܣ��٣�
�ʴ�Ϊ���ڣ��ۣ��ܣ��٣�
���� ���⿼���Ϊ�ۺϣ��漰�ε�ˮ��ԭ���������Ƽ����ѧƽ�⼰��Ӱ���֪ʶ����Ŀ�Ѷ��еȣ���ȷ�ε�ˮ��ԭ����Ӱ�컯ѧƽ�������Ϊ���ؼ�������������ѧ���ķ������������Ӧ��������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һȥ���ۣ�CO32-+H2O�THCO3-+OH- | |
| B�� | ��ĭ���������ԭ����2Al3++3CO32-+3H2O�T2A1��OH��3��+3CO2�� | |
| C�� | ������Һ�м������������������Һ��Al3++SO42-+Ba2++4OH-�TBaSO4��+AlO2-+2H2O | |
| D�� | ��ʯīΪ�缫�����Pb��NO3��2��Cu��NO3��2�Ļ����Һ��ȡPbO2ʱ�������Ϸ����ĵ缫��Ӧʽ��Pb2++2 H2O-2e-�TPbO2+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȳ�ĽṹʽΪCH��CH | B�� | ������ӵı���ģ��Ϊ | ||
| C�� | ̼ԭ�ӵĽṹʾ��ͼΪ  | D�� | ̼ԭ���������ӵĹ����ʾʽΪ 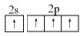 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
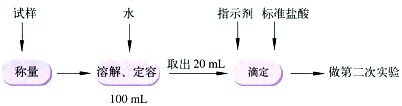
| ���� | ��Ʒ | ���ĵ�ϡ���� | ��Ӧ�����Һ |
| ������g�� | 4.5g | 37.7g | 40g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������γ����Ӽ���������γɹ��ۼ� | |
| B�� | �����KI��Һ�еμ���ˮ����Һ���� | |
| C�� | ��Na2SO3��Һ�еμ����ᣬ���������� | |
| D�� | F2�ڰ�����H2����ը��I2�ڰ�����H2��������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ��Ӧ | B�� | ������Ӧ | C�� | �ӳɷ�Ӧ | D�� | �ۺϷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca��Mg��Na | B�� | Cl-��S2-��O2- | C�� | P3-��S2-��Cl- | D�� | K+��Cl-��S2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
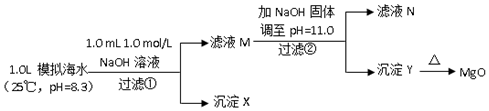
| ģ�⺣ˮ�е�����Ũ��/ ��mol/L�� | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com