
| A.①④⑤⑥⑦⑧ | B.①②④⑤ | C.①④⑤⑥ | D.全部 |
科目:高中化学 来源:不详 题型:实验题
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 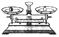 |  |  |  |  | 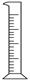 |
| 序号 | a | b | c | d | e | f |
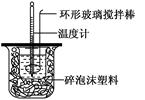
| 温度 实验次数 | 超始温度t1/℃ | 终止温度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用饱和Na2CO3溶液可除去二氧化碳中的氯化氢 |
| B.铜粉中含有少量的氧化铜,可加入稀硝酸后过滤 |
| C.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中 |
| D.配制浓硫酸和浓硝酸混酸时,应将浓硫酸慢慢加到浓硝酸中,并及时搅拌和冷却 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.450 mL,52.7 g | B.500 mL,58.5 g |
| C.450 mL,58.5 g | D.500 mL,52.7 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.纸层析实验中若选择水做固定相,有机溶剂做流动相,则亲水性强的成分在流动相中分配的少一些,在毛细现象作用下,随流动相移动的速度快一些 |
| B.判断CuO和MnO2对H2O2分解的催化效率,可通过比较H2O2溶液析出气泡的快慢程度,或测定单位时间内产生氧气的体积 |
| C.食醋总酸含量测定实验中,实验结束时碱式滴定管尖嘴部位有气泡,则测定的醋酸含量偏高 |
| D.将硫酸亚铁和硫酸铵的混合溶液加热浓缩,冷却结晶后可析出摩尔盐粗产品,再用酒精洗去晶体表面的水分,加热烘干后称重,计算产率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 Na2S2O3,
Na2S2O3,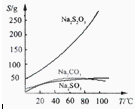
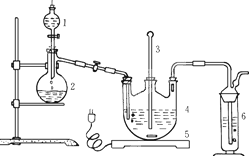
| A.BaCl2溶液 | B.浓H2SO4 |
| C.酸性KMnO4溶液 | D.NaOH溶液 |
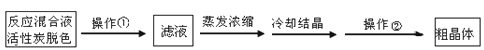
 6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应: I2+2S2O32-=2I-+S4O62-,滴定终点的现象为 ,
6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应: I2+2S2O32-=2I-+S4O62-,滴定终点的现象为 ,查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
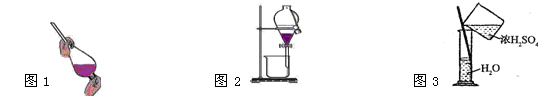
| A.萃取操作时,振荡过程中需要放气,放气是通过打开分液漏斗上口的玻璃塞进行的 |
| B.可以采用蒸发浓缩、冷却结晶的方法从硝酸钾溶液中获得硝酸钾晶体 |
| C.将乙醇与水分离,如图1、图2操作 |
| D.稀释浓H2SO4,如图3操作 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com