
I2+SO2+2H2O====H2SO4+2HI
2FeCl2+Cl2====2FeCl3
2FeCl3+2HI====2FeCl2+2HCl+I2
A.I->Fe2+>Cl->SO2 B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.SO2>I->Fe2+>Cl-
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| ||
| ||
| ||
| ||
| CuO/ZnO |
| 1 |
| 2 |
| c(CH3OH) |
| c(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
“氢能”将是未来最理想的新能源。
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
A.2H2(g)+O2(g) ![]() 2H2O(l) △H= -142.9kJ·mol—1
2H2O(l) △H= -142.9kJ·mol—1
B.H2(g)+1/2 O2(g) ![]() H2O(l) △H= -285.8kJ·mol—1
H2O(l) △H= -285.8kJ·mol—1
C.2H2+O2![]() 2H2O(l) △H= -571.6kJ·mol—1
2H2O(l) △H= -571.6kJ·mol—1
D.H2(g)+1/2O2(g) ![]() H2O(g) △H= -285.8kJ·mol—1
H2O(g) △H= -285.8kJ·mol—1
Ⅱ.某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤
①CaBr2+H2O![]() CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg![]() HgBr2+H2
HgBr2+H2
③HgBr2+_____![]() ______________ ④2HgO
______________ ④2HgO 2Hg+O2↑
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:____________。
根据“绿色化学”的思想评估该方法制H2的主要缺点:______________。
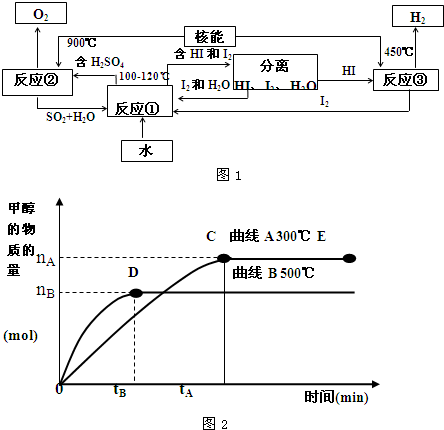
Ⅲ.利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。(提示:反应②的产物是O2、SO2和H2O)

完成下列反应的化学方程式:
反应①__________________________;反应②__________________________。
此法制取氢气的最大优点是_______________________________________________。
Ⅳ.氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g) CO2(g)+ H2(g); △H<0。
在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2 和 x mol H2,则:
①当x=5.0时,上述平衡向___________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
(3)在850℃时,若设x=5.0mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a_______ b(填“大于”、“小于”或“等于”)。
Ⅴ.氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。
(1)现有8克氧化铜被氢气还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.8克上述混合物与足量的稀硫酸充分反应后过滤,可得到固体 g;
(3)若将6.8克上述混合物与一定量的浓硝酸充分反应,
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68g。经分析,原溶液中的Cu2+有20%残留在母液中。求所得晶体的化学式
查看答案和解析>>
科目:高中化学 来源:2012届浙江省东阳中学高三下学期阶段检测化学试卷 题型:填空题
“氢能”将是未来最理想的新能源。
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
A.2H2(g)+O2(g)  2H2O(l)△H= -142.9kJ·mol—1 2H2O(l)△H= -142.9kJ·mol—1 |
B.H2(g)+1/2 O2(g)  H2O(l)△H= -285.8kJ·mol—1 H2O(l)△H= -285.8kJ·mol—1 |
C.2H2+O2 2H2O(l)△H= -571.6kJ·mol—1 2H2O(l)△H= -571.6kJ·mol—1 |
D.H2(g)+1/2 O2(g)  H2O(g) △H= -285.8kJ·mol—1 H2O(g) △H= -285.8kJ·mol—1 |
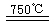 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg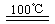 HgBr2+H2
HgBr2+H2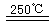 ______________ ④2HgO
______________ ④2HgO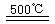 2Hg+O2↑
2Hg+O2↑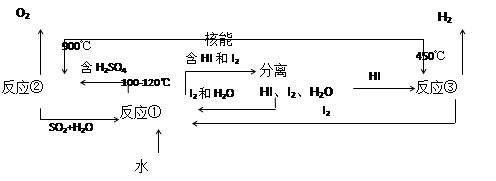
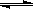 CO2(g)+ H2(g); △H<0。
CO2(g)+ H2(g); △H<0。查看答案和解析>>
科目:高中化学 来源:2014届湖北省襄阳市四校联考高一下学期期中考试化学试卷(解析版) 题型:填空题
(8分)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 ,A的最高价氧化物的化学式
是 。
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写) 。
(3)E的最高价氧化物对应的水化物与C的最高价氧化物对应的水化物发生反应的化学方
程式是 。
(4)简述比较D与E金属性强弱的实验方法; 。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省高三上学期期中考试(化学) 题型:填空题
(8分)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 ,A的最高价氧化物的化学式
是 。
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写) 。
(3)E的最高价氧化物对应的水化物与C的最高价氧化物对应的水化物发生反应的化学方
程式是 。
(4)简述比较D与E金属性强弱的实验方法; 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com