
【题目】氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途。
完成下列填空:
(1)实验室配制氯化铝溶液时加入盐酸的目的是______________________________________________。
(2)往AlCl3溶液中加入过量下列溶液,最终得到无色澄清溶液的是________(选填编号)。
a.Na2CO3 b.NaOH c.NaAlO2 d.H2SO4
(3)用滴管向试管中滴加少量AlCl3溶液时,滴管不得伸入试管中的理由是__________________,用试管夹夹持上述试管在酒精灯上加热时,不断上下移动试管的目的是____________________________。取AlCl3溶液,用小火持续加热至水刚好蒸干,生成白色固体为________。
(4)为确定Al2(OH)nCl(6-n)中n的值,取3.490 g白色固体,全部溶解在0.112 0 mol的HNO3(足量)中,并加水稀释成100 mL,将溶液分成两等份,进行如下实验:
①一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得Al2O3的质量为1.020 g,判断加入氨水已足量的操作是________。过滤、洗涤后至少要灼烧________次(填写数字);测定样品中铝元素含量时不选择测定干燥Al(OH)3的质量,而是测定Al2O3的质量的原因可能是________(选填编号)。
a.干燥Al(OH)3固体时易失水
b.Al2O3的质量比Al(OH)3大,误差小
c.沉淀Al(OH)3时不完全
d.灼烧氧化铝时不分解
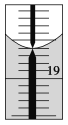
②从另一份溶液中取出20.00 mL,用0.129 0 mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00 mL,终点时滴定管液面(局部)如图所示(背景为白底蓝线的滴定管)。则滴定管的读数________ mL,Al2(OH)nCl(6-n)中n的值为________。
【答案】防止氯化铝水解bd防止试剂被污染防止局部受热引起暴沸Al(OH)3静置,取上层清液,滴加氨水,无沉淀生成2ad18.605
【解析】
(1).氯化铝水解使溶液显酸性;(2).a、AlCl3和Na2CO3发生双水解;b、AlCl3和过量的氢氧化钠反应生成NaAlO2;c、AlCl3和NaAlO2发生双水解;d、AlCl3和硫酸不反应.(3).向试管中滴加溶液时应“垂直、悬空”,用试管夹夹持上述试管在酒精灯上加热时,要上下移动试管防止局部暴沸;AlCl3溶液蒸干时水解被促进,得Al(OH)3;(4).判断试剂已过量的方法是继续滴加,当氨水加入过量时,取上层清液继续滴加氨水,则无沉淀生成;将所得的Al(OH)3沉淀至少灼烧2-3次,至两次质量差不超过0.1g即说明Al(OH)3分解完全得Al2O3,不选择测定干燥Al(OH)3的质量,而是测定Al2O3的质量的原因是Al(OH)3热稳定性不如Al2O3好;(5).滴定管的0刻度在上,根据0.1120mol HNO3的消耗有两个原因:被3.490g Al2(OH)nCl(6-n)中OH-消耗的和被0.1290mol/L的标准NaOH溶液消耗的,据此计算。
解析:(1).氯化铝水解使溶液显酸性,加入盐酸能抑制其水解,故答案为:防止氯化铝水解;(2).a.AlCl3和Na2CO3发生相互促进水解反应:2AlCl3+3Na2CO3+3H2O=2Al(OH)3↓+3CO2↑,得不到澄清溶液,故a错误;b.AlCl3和过量的氢氧化钠反应生成NaAlO2溶液,反应方程式为AlCl3+4NaOH=3NaCl+NaAlO2+2H2O,得澄清溶液,故b正确;c.AlCl3和NaAlO2发生相互促进水解,反应方程式为AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,得不到澄清溶液,故c错误;d.AlCl3和硫酸不反应,溶液仍为澄清,故d正确,答案选bd;
(3).向试管中滴加溶液时应“垂直、悬空”,目的是防止污染试剂;用试管夹夹持上述试管在酒精灯上加热时,要上下移动试管防止局部暴沸;AlCl3溶液蒸干时由于水解生成的HCl是挥发性酸,HCl的挥发导致水解被促进,故最终得Al(OH)3;故答案为:防止试剂被污染;防止局部受热引起暴沸;Al(OH)3;
(4).①.判断试剂已过量的方法是继续滴加,即当氨水加入过量时,取上层清液继续滴加氨水,则无沉淀生成;将所得的Al(OH)3沉淀至少灼烧2~3次,至两次质量差不超过0.1 g即说明Al(OH)3分解完全得Al2O3,不选择测定干燥Al(OH)3的质量,而是测定Al2O3的质量的原因是干燥Al(OH)3时易分解失水,而灼烧Al2O3不失水,故答案为:静置,取上层清液,滴加氨水,无沉淀生成;2;ad;
②.滴定管的0刻度在上,故滴定管的读数为18.60 mL,则消耗的氢氧化钠的体积为18.60 mL;根据0.112 0 mol HNO3的消耗有两个原因:被3.490 g Al2(OH)nCl(6-n)中OH-消耗的和被0.129 0 mol/L的标准NaOH溶液消耗的,可有:0.112 mol=![]() ×n mol+0.129 mol/L×0.018 6 L×5,解得n=5,故答案为:18.60;5。
×n mol+0.129 mol/L×0.018 6 L×5,解得n=5,故答案为:18.60;5。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】碳是一种极其重要的元素,工业上,生活中到处可见。
(1)碳原子核外有________种能量不同的电子,这些电子占据了______个纺锤形轨道。
(2)下列方法可以比较碳与硫的非金属性强弱的是__________
a.比较原子最外层电子数多少 b.比较其最高价氧化物对应水化物的酸性
c.比较气态氢化物的稳定性 d.比较单质的熔沸点高低
(3)煤的气化是煤高效洁净利用的方向之一。在一定温度下的某容积可变的密闭容器中 建立下列化学平衡:C(s)+H2O(g)![]() CO(g)+H2(g)-Q,可认定该可逆反应在一定条件下已达到化学平衡状态的是_____(选填序号)。
CO(g)+H2(g)-Q,可认定该可逆反应在一定条件下已达到化学平衡状态的是_____(选填序号)。
a.体系的压强不再发生变化 b.v正(CO)=v逆(H2O)
c.生成n molCO的同时生成n mol H2 d.1mol H-H键断裂同时断裂2mol H-O键
(4)若上述化学平衡状态从正反应开始建立,达到平衡后,给平衡体系加压(缩小体积),则容器内气体的平均相对分子质量将______(填写不变、变小、变大、无法确定)。若工业上以此方法生产水煤气,提高产率的措施为____。(写出两条措施)
(5)空气中的CO2浓度增大,会导致温室效应,有人提出将CO2通过管道输送到海底,这可减缓空气中CO2浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。请你结合CO2的性质,从平衡角度分析酸性增强原因 _____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2的烟气会危害环境。利用工业废碱渣(主要成分Na2CO3)可吸收烟气中的SO2并制备无水Na2SO3,其流程如图。
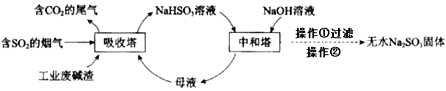
下列说法中不正确的是
A.吸收塔中的温度不宜过高,原因可能是防止SO2的溶解度下降
B.为提高NaHSO3的产率,应控制吸收塔中溶液为弱碱性
C.吸收塔中生成HSO3-的离子方程式是2SO2+CO32-+H2O=2HSO3-+CO2↑
D.操作②为蒸馏水洗涤、干燥,得无水Na2SO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
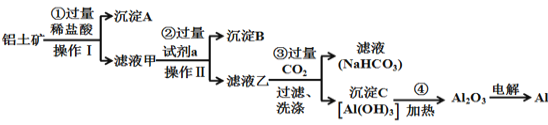
(1)在操作Ⅰ之前先将铝土矿研磨成粉末,目的是:___________________;
(2)沉淀A的化学式是__________;
(3)步骤③中通入过量CO2,产生沉淀C的离子方程式为_________________________;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为____________;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是___________;
a. MgO b. V2O5 c. Fe3O4 d. MnO2
(6)我国首创以铝—空气—海水电池为能源的新型电池,用作海水标志灯已研制成功。该电池以取之不尽的海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流。负极材料是铝,正极材料可以用石墨。写出正极电极反应式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgI在水中的沉淀溶解平衡曲线如图所示,又知t℃时AgBr的Ksp=5×10-13。下列说法不正确的是( )
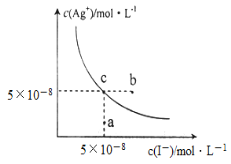
A.在t℃时,AgI的Ksp=2.5×10-15 mol2.L-2
B.图中b点有碘化银晶体析出
C.向c点溶液中加入适量蒸馏水,可使溶液由c点到a点
D.在t℃时,反应AgBr(s)+I-(aq)![]() AgI(s)+Br-(aq)的平衡常数K=200
AgI(s)+Br-(aq)的平衡常数K=200
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷的分子结构可简写成键线型结构![]() 。有机物A的键线式结构为
。有机物A的键线式结构为![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是
,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是
A.有机物A的一氯代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C.有机物A的分子式为C8H15
D.B的结构可能有3种,其中一种的名称为3,4,4-三甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某浓度的硝酸与过量铁粉反应,生成4.48 L N2O气体(标准状况下),若改与铝反应(生成NO气体),则最后可溶解的铝的质量是
A.27 gB.9 gC.13.5 gD.8.9 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(s)cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )

A. 根据图象无法确定改变温度后平衡移动方向
B. 使用催化剂,C的物质的量分数增加
C. 化学方程式系数a>c+d
D. 升高温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物在生产生活中有广泛应用,其吸收处理也十分重要。
(1)完成并配平下列离子方程式_____。
Fe3++ SO2+ → Fe2++ SO42-+
(2)标明电子转移的方向和数目______: Fe3++ SO2……。
(3)在Na2SO3溶液中滴加酚酞,溶液呈红色,若在该溶液中滴入过量的BaCl2溶液,实验现象为:_____。请结合离子方程式,运用平衡原理进行解释_____。
(4)在NaClO溶液中通入SO2,写出反应的离子方程式:_____。
(5)在0.1mol/LNa2SO3溶液中,下列关系式正确的是_____。
a.[Na+]+[H+]=[SO32-]+[HSO3-]+[OH-] b.[Na+]>[SO32-]>[OH-]>[H+]
c.[Na+]=2[SO32-]+2[HSO3-]+2[H2SO3] d.[Na+]=2[SO32-]>[OH-]=[H+]
(6)向该溶液中加入少量Na2SO3固体,![]() ___(填“增大”“减小”或“不变”)。
___(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com