
| A£® | YĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚ2ÖÜĘŚµŚIVA×å | |
| B£® | X”¢Y”¢Z”¢W”¢MµÄŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖM£¾Y£¾Z£¾W£¾X | |
| C£® | X”¢Z”¢WŠĪ³ÉµÄŃĪÖŠÖ»ŗ¬ÓŠĄė×Ó¼ü | |
| D£® | ²śÉś“Ģ¼¤ŠŌĘųĪ¶ĘųĢåµÄ·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖH++HSO3-=H2O+SO2”ü |
·ÖĪö ŌŖĖŲX”¢Y”¢Z”¢W”¢M”¢NµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬Z2X4æÉŅŌ×÷»š¼żČ¼ĮĻ£¬X2W2ĪŖ18µē×Ó·Ö×Ó£¬ŌņZĪŖN£¬XĪŖH£»ŌŚ»ÆŗĻĪļY2X2”¢Z2X4”¢X2W2ÖŠĻąÓ¦·Ö×ÓÄŚø÷Ō×Ó×īĶā²ćµē×Ó¶¼Āś×ćĪČ¶Ø½į¹¹£¬YĪŖC£¬WĪŖO£¬½įŗĻXÓėM”¢WÓėN·Ö±šĶ¬Ö÷×壬ĒŅŌŖĖŲX”¢Y”¢Z”¢W·ÖŹōĮ½øö¶ĢÖÜĘŚ£¬ĖüĆĒĖÄÕßµÄŌ×ÓŠņŹżÖ®ŗĶĪŖ22£¬×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ16£¬ŌņMĪŖNa£¬NĪŖS£¬¾łŗ¬X”¢W”¢M”¢NĖÄÖÖŌŖĖŲµÄĮ½ÖÖ³£¼ū»ÆŗĻĪļĻą»„·“Ó¦ÓŠ“ų“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢå·Å³ö£¬ĪŖĮņĖįĒāÄĘÓėŃĒĮņĖįĒāÄĘ·“Ӧɜ³ÉĘųĢ嶞Ńõ»ÆĮņ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗŌŖĖŲX”¢Y”¢Z”¢W”¢M”¢NµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬Z2X4æÉŅŌ×÷»š¼żČ¼ĮĻ£¬X2W2ĪŖ18µē×Ó·Ö×Ó£¬ŌņZĪŖN£¬XĪŖH£»ŌŚ»ÆŗĻĪļY2X2”¢Z2X4”¢X2W2ÖŠĻąÓ¦·Ö×ÓÄŚø÷Ō×Ó×īĶā²ćµē×Ó¶¼Āś×ćĪČ¶Ø½į¹¹£¬YĪŖC£¬WĪŖO£¬½įŗĻXÓėM”¢WÓėN·Ö±šĶ¬Ö÷×壬ĒŅŌŖĖŲX”¢Y”¢Z”¢W·ÖŹōĮ½øö¶ĢÖÜĘŚ£¬ĖüĆĒĖÄÕßµÄŌ×ÓŠņŹżÖ®ŗĶĪŖ22£¬×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ16£¬ŌņMĪŖNa£¬NĪŖS£¬¾łŗ¬X”¢W”¢M”¢NĖÄÖÖŌŖĖŲµÄĮ½ÖÖ³£¼ū»ÆŗĻĪļĻą»„·“Ó¦ÓŠ“ų“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢå·Å³ö£¬ĪŖĮņĖįĒāÄĘÓėŃĒĮņĖįĒāÄĘ·“Ӧɜ³ÉĘųĢ嶞Ńõ»ÆĮņ£¬
A£®YĪŖC£¬Ī»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚ2ÖÜĘŚµŚIVA×壬¹ŹAÕżČ·£»
B£®µē×Ó²ćŌ½¶ą£¬Ō×Ó°ė¾¶Ō½“ó£¬Ķ¬ÖÜĘŚ“Ó×óĻņÓŅŌ×Ó°ė¾¶¼õŠ”£¬ŌņX”¢Y”¢Z”¢W”¢MµÄŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖM£¾Y£¾Z£¾W£¾X£¬¹ŹBÕżČ·£»
C£®X”¢Z”¢WŠĪ³ÉµÄŃĪĪŖĻõĖįļ§£¬ŗ¬ÓŠĄė×Ó¼üŗĶ¹²¼Ū¼ü£¬¹ŹC“ķĪó£»
D£®ĮņĖįĒāÄĘÓėŃĒĮņĖįĒāÄĘ·“Ӧɜ³ÉĘųĢ嶞Ńõ»ÆĮņ£¬²śÉś“Ģ¼¤ŠŌĘųĪ¶ĘųĢåµÄ·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖH++HSO3-=H2O+SO2”ü£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌ×Ó½į¹¹”¢ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶ĶʶĻŌŖĖŲµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėĶʶĻÄÜĮ¦µÄ漲飬עŅāÖÜĘŚĀɼ°ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
 Ķعżµē½ā±„ŗĶŹ³ŃĪĖ®µĆµ½µÄĒāŃõ»ÆÄĘ¹ĢĢåѳʷ³£ŗ¬ÓŠĀČ»ÆÄĘŌÓÖŹ£®Ą“Ą“Ķ¬Ń§ĄūÓĆÖŠŗĶµĪ¶ØŌĄķ²ā¶ØĒāŃõ»ÆÄʵÄÖŹĮæ·ÖŹż£®²½ÖčĪŖ£ŗ
Ķعżµē½ā±„ŗĶŹ³ŃĪĖ®µĆµ½µÄĒāŃõ»ÆÄĘ¹ĢĢåѳʷ³£ŗ¬ÓŠĀČ»ÆÄĘŌÓÖŹ£®Ą“Ą“Ķ¬Ń§ĄūÓĆÖŠŗĶµĪ¶ØŌĄķ²ā¶ØĒāŃõ»ÆÄʵÄÖŹĮæ·ÖŹż£®²½ÖčĪŖ£ŗ| ŹµŃéŠņŗÅ | “ż²āѳʷČÜŅŗĢå»ż£ØmL£© | µĪ¶Ø¹Ü¶ĮŹż | Ļūŗıź×¼ŃĪĖįČÜŅŗµÄĢå»ż£ØmL£© | |
| ³õ¶ĮŹż | Ä©¶ĮŹż | |||
| 1 | 20.00 | 0.00 | 19.95 | 19.95 |
| 2 | 20.00 | 0.05 | 19.90mL | 19.85mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
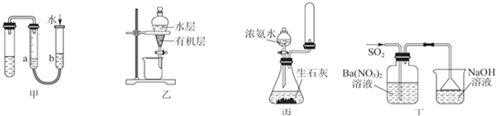
| A£® | ÓĆĶ¼¼×µÄ·½·Ø²»Äܼģ²é“Ė×°ÖƵÄĘųĆÜŠŌ | |
| B£® | Ķ¼ŅŅæÉŅŌ×÷ĪŖCCl4ŻĶČ”äåĖ®ŗóµÄ·ÖŅŗ×°ÖĆ | |
| C£® | ŹµŃéŹŅÓĆĶ¼±ūĖłŹ¾×°ÖĆÖĘȔɣĮæ°±Ęų | |
| D£® | Ķ¼¶”Ļ“ĘųĘæÖŠµÄ°×É«³ĮµķĪŖBaSO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
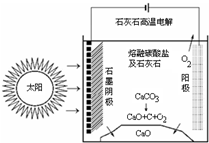 CO2ŹĒŗĻ³ÉÄņĖŲµÄŌĮĻ£¬µ«Ė®Äą³§Éś²śŹ±Č“Åŷųö“óĮæµÄCO2£®»ŖŹ¢¶Ł“óѧµÄŃŠ¾æČĖŌ±ŃŠ¾æ³öŅ»ÖÖ·½·Ø£¬æÉŹµĻÖĖ®ÄąÉś²śŹ±CO2ĮćÅÅ·Å£¬Ę仳±¾ŌĄķČēĶ¼ĖłŹ¾£ŗ
CO2ŹĒŗĻ³ÉÄņĖŲµÄŌĮĻ£¬µ«Ė®Äą³§Éś²śŹ±Č“Åŷųö“óĮæµÄCO2£®»ŖŹ¢¶Ł“óѧµÄŃŠ¾æČĖŌ±ŃŠ¾æ³öŅ»ÖÖ·½·Ø£¬æÉŹµĻÖĖ®ÄąÉś²śŹ±CO2ĮćÅÅ·Å£¬Ę仳±¾ŌĄķČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®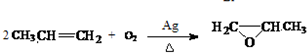 £®
£®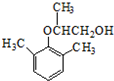 £®
£®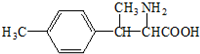 £®
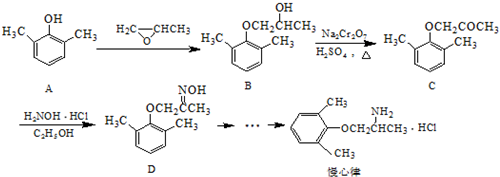
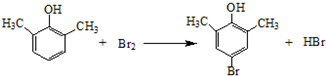
£®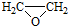 £©£®Š“³öŅŌĮŚ¼×»ł±½·Ó £Ø
£©£®Š“³öŅŌĮŚ¼×»ł±½·Ó £Ø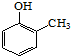 £©ŗĶŅŅ“¼ĪŖŌĮĻÖʱø
£©ŗĶŅŅ“¼ĪŖŌĮĻÖʱø 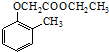 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH3CH2OH$”ś_{170”ę}^{ÅØH_{2}SO_{4}}$CH2=CH2£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH3CH2OH$”ś_{170”ę}^{ÅØH_{2}SO_{4}}$CH2=CH2£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
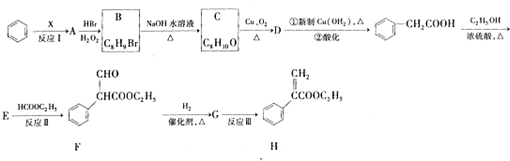
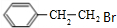 £»EµÄ·Ö×ÓŹ½ĪŖC10H12O2£»FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»łŗĶõ„»ł£®
£»EµÄ·Ö×ÓŹ½ĪŖC10H12O2£»FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»łŗĶõ„»ł£® £®
£® Öʱø
Öʱø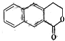 µÄŗĻ³ÉĀ·Ļß
µÄŗĻ³ÉĀ·Ļß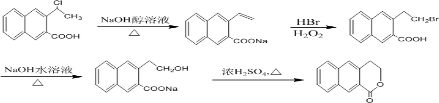 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
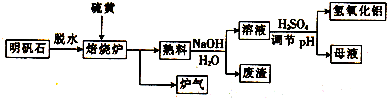
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
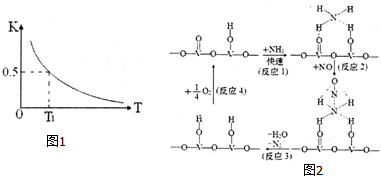 »·¾³ĪŪČ¾Ó°ĻģČĖĄąÉś“ę£¬ÖĪĄķĪŪČ¾ŹĒ»Æѧ¹¤×÷ÕßŃŠ¾æµÄÖŲŅŖæĪĢā£®
»·¾³ĪŪČ¾Ó°ĻģČĖĄąÉś“ę£¬ÖĪĄķĪŪČ¾ŹĒ»Æѧ¹¤×÷ÕßŃŠ¾æµÄÖŲŅŖæĪĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1Ļī | B£® | 2Ļī | C£® | 3Ļī | D£® | 4Ļī |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com