
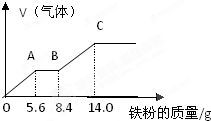
 ijϡ�����ϡ����Ļ����Һ100mL���������������ۣ�������������������������ӵı仯��ͼ��ʾ����֪����Ļ�ԭ����ֻ��NO���壩
ijϡ�����ϡ����Ļ����Һ100mL���������������ۣ�������������������������ӵı仯��ͼ��ʾ����֪����Ļ�ԭ����ֻ��NO���壩| 5.6g |
| 56g/mol |
| 14g |
| 56g/mol |
| 0.25mol |
| 0.1L |
| 8.4g-5.6g |
| 56g/mol |
| 5.6g |
| 56g/mol |
| 3 |
| 2 |


 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ֻ���Ǽ��Լ��ķ���һ���ǷǼ��Է��� |
| B�����м��Լ��ķ���һ���Ǽ��Է��� |
| C���Ǽ��Է���һ�����зǼ��Լ� |
| D���ɼ��Լ����ɵ�˫ԭ�ӷ���һ���Ǽ��Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���Ȼ���ĵ���ʽH+[��
| ||||
B��þ��ԭ�ӽṹʾ��ͼ | ||||
| C��������Ľṹʽ H-Cl-O | ||||
| D��ʵ������ȡ���������ӷ���ʽMnO2+4HCl��Ũ��=Cl2+Mn2++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| L/min | 0 | 2 | 4 | 6 | 8 | �� | 16 | 18 |
| n��X��/mol | 1.600 | 1.200 | 1.100 | 1.075 | �� | �� | 1.000 | 1.000 |
| c2(Z) |
| c(X)?c(Y) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��CO32-��Cl- |
| B��Mg2+��Ba2+��Br- |
| C��Ag+��Na+��Cl- |
| D��Na+��NH4+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

 �������Ʊ�һ����Ҫ���л�����ԭ��ˮ����
�������Ʊ�һ����Ҫ���л�����ԭ��ˮ���� ��ʹ������ͼ��ʾ���Ʊ����̣�������ͼʾ����CH3CH2OH
��ʹ������ͼ��ʾ���Ʊ����̣�������ͼʾ����CH3CH2OH| Ũ���� |
| 170�� |
| Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��B��C��X��Ϊ��ѧ��ѧ��������һ����������������ͼת����ϵ��������������ȥ��������˵����ȷ���ǣ�������
A��B��C��X��Ϊ��ѧ��ѧ��������һ����������������ͼת����ϵ��������������ȥ��������˵����ȷ���ǣ�������| A����XΪFe����C����ΪFe��NO3 ��2 |
| B����XΪKOH��Һ����A����ΪAl |
| C����XΪO2����A��Ϊ�л����Ҵ���Ҳ��Ϊ�ǽ��������� |
| D����A��B��C��Ϊ��ɫ��Ӧ�ʻ�ɫ�Ļ������Xһ��ΪCO2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com