
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρg·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①
②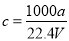
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④将50g上述溶液加入一定量的水稀释成0.5 c mol·L-1,则加入水的体积应大于50mL
A.①④ B.②③ C.①③ D.②④
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
下列反应的能量变化与其他三项不相同的是
A.铝粉与氧化铁的反应
B.NH4Cl晶体与Ba(OH)2·8H2O晶体的反应
C.锌片与稀硫酸反应
D.钠与冷水反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第一次五校联考化学试卷(解析版) 题型:填空题
(10分)金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。

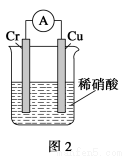
(1)铜铬构成原电池如右图1,其中盛稀硫酸烧杯中的现象为: 。盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是:
A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
(2)如构成图2电池发现,铜电极上不再有图1的现象,铬电极上产生大量气泡,遇空气呈红棕色。写出正极电极反应式: 。
(3)某同学把已去掉氧化膜的铬片直接投入氯化铜溶液时,观察到了预料之外的现象:①铬片表面上的铜没有紧密吸附在铬片的表面而是呈蓬松的海绵状;②反应一段时间后有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,证明是氢气。请解释这两种现象的原因___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第一次五校联考化学试卷(解析版) 题型:选择题
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是
序号 | 甲 | 乙 | 丙 |
① | CO2 | SO2 | 石灰水 |
② | HCl | CO2 | 石灰水 |
③ | CO2 | SO2 | Ba(NO3)2 |
④ | NO2 | SO2 | BaCl2 |
⑤ | CO2 | NH3 | CaCl2 |
A.②③④ B.②③④⑤ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:实验题
(12分)为测定某混合物中各组分的质量分数(已知该混合物含NaCl、Na2CO3?10H2O和NaHCO3),设计如下:

实验:
(1)加热前通入空气的目的是 ______________,操作方法为_______________________________。
(2)装置C中盛放的试剂可以是___________(填序号)。
a.碱石灰 b.无水CaCl2 c.P2O5 d.固体NaOH
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将________(填“偏高”、“偏低”或“无影响”,下同);若撤去E装置,则测得Na2CO3?10H2O的含量 。
(4)若样品质量为 w g,反应后C、D增加的质量分别为 m1 g、m2 g,由此可知混合物中NaHCO3质量分数为_____________________(用含w、m1、m2的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y、Z的原子序数依次增大,W、X的最外层电子数之比为4︰3,Y原子的最外层电子数是次外层电子数的一半,Z元素原子的半径在同周期元素原子中最小。下列叙述正确的是
A.W、X、Y的最高价氧化物都能与NaOH溶液反应,它们都属于酸性氧化物
B.W、Y、Z三种元素简单气态氢化物的热稳定性为: Z>W>Y
C.Z元素最高价氧化物对应的水化物的化学式为HZO3
D.原子半径的大小顺序为:rY>rW>rX
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:选择题
下列有关试剂的保存方法,错误的是
A.浓硝酸保存在无色玻璃试剂瓶中
B.少量的钠保存在煤油中
C.氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中
D.新制的氯水通常保存在棕色玻璃试剂瓶中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.25℃时,pH=13的氨水中含有OH-的数目为0.1NA
B.标准状况下,2.24 LNO2 与水反应生成NO3-的数目为0.1NA
C.1 mol Na被完全氧化生成Na2O2,转移电子的数目为NA
D.4.0 g H2与足量O2完全反应生成水,反应中断裂共价键的总数为2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省枣阳市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
①某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了 ,B元素位于周期表五个区域中的 区。

②ACl2分子中A的杂化类型为 ,ACl2的空间构型为 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
②六氰合亚铁离子[Fe(CN)6]4—中不存在 。
A.共价键
B.非极性键
C.配位键
D.σ键
E.π键
③写出一种与 CN—互为等电子体的单质分子式 。
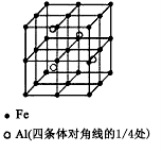
(3)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
①确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com