

 ��Ca��OH��2�ܺ�п���ӷ�����Ӧ����������п��
��Ca��OH��2�ܺ�п���ӷ�����Ӧ����������п�� ����ֹ����Zn��OH��2��
����ֹ����Zn��OH��2��

 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| c3(H+) |
| c(Fe3+) |
| c3(H+) |
| c(Fe3+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�ձ����и����ڶ��ε��в��Ի�ѧ�Ծ��������棩 ���ͣ������
����п���Ʊ�ӫ��۵�ԭ��֮һ����ҵ����п����Ҫ�ɷ���ZnO��������Fe2O3��CuO��SiO2�����ʣ��Ʊ�ZnSO4•7H2O���������¡�
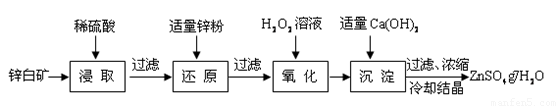
��֪�������£���Һ�е�Fe3+��Zn2+��Fe2+������������ʽ��ȫ������pH�ֱ�Ϊ��3.7��6.5��9.7��
��1����ȡ��������߽���Ч�ʿɲ��õĴ�ʩ���������δ�һ������
ZnO�����ᷴӦ�Ļ�ѧ����ʽΪ������
��2����������п�۵�����Ϊ����ʹ��Һ�е�Fe3+ת��ΪFe2+����������
��3������������H2O2������Ӧ�����ӷ���ʽΪ������
��4����������Ca(OH)2������ҺpH���ٽ�Fe3+ˮ�⣬Fe3+ˮ�ⷴӦ��ƽ�ⳣ������ʽ
K��������Ca(OH)2���ܹ�����ԭ����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com