
(共5分,每空1分)测得某溶液的pH = 6.5,且氢离子与氢氧根离子物质的量相等,此溶液呈_____性。测定温度______室温(填高于、低于或等于),其理由是 。 将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合。
(1)若所得混合液为中性,则a︰b 。
(2)若所得混合液的pH=2,则a︰b 。
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
(本题共6分,每空1分)请同学们根据官能团的不同对下列有机物进行分类。
(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;
(5)醛: ;(6)酯: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(17分,每空1分,特别说明的除外)下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ______,⑥ ______,⑦ __ __。
(2)画出原子的结构示意图:④___ __ ___,⑧___ 。
(3)在①~12元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (填序号),跟它同周期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省龙东南六校高二下学期期末联考化学试题 题型:填空题
(本题共6分,每空1分)请同学们根据官能团的不同对下列有机物进行分类。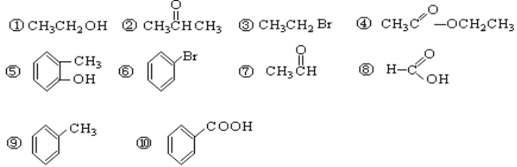
(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;
(5)醛: ;(6)酯: 。
查看答案和解析>>
科目:高中化学 来源:2010年黑龙江省龙东南六校高二下学期期末联考化学试题 题型:填空题
(本题共6分,每空1分)请同学们根据官能团的不同对下列有机物进行分类。
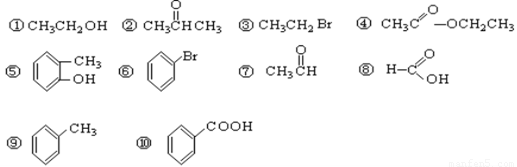
(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;
(5)醛: ;(6)酯: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(本题共6分,每空1分)请同学们根据官能团的不同对下列有机物进行分类。
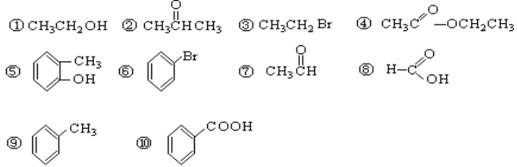
(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;
(5)醛: ;(6)酯: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com