
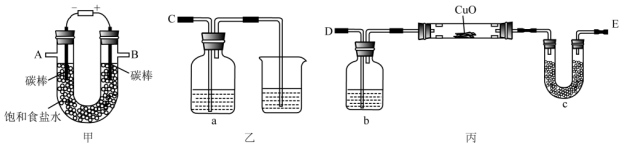
分析 (1)用还原性物质检验氯气,氢气与氧化铜反应生成水,根据干燥管的质量变化计算水,进而计算铜;
(2)氯气具有氧化性,能使淀粉碘化钾溶液变蓝色;
(3)电解饱和食盐水产生的氢气中含有水蒸气,会影响铜的相对原子质量的测定,必须干燥.
解答 解:(1)电解饱和食盐水时,电解反应离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,B出口是氯气,要检验氯气的氧化性,则氯气连接强还原性的物质且反应现象要明显,故B连接C;A出口为氢气,氢气与氧化铜反应生成水,根据干燥管的质量变化计算水,进而计算铜,因为电解得到的氢气中含有水蒸气,所以在实验前要除去水蒸气,故A连接D,
故答案为:D;C;
(2)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是碘化钾淀粉溶液,氯气与碘化钾反应生成单质碘,溶液会变蓝色;
故答案为:碘化钾淀粉溶液;溶液变蓝色;
(3)b中是浓硫酸,用于干燥氢气;防止在实验时,氢气中含有水蒸气,影响铜的相对原子质量的测定;
故答案为:浓硫酸;干燥氢气.
点评 本题考查较为综合,涉及性质实验设计以及相对原子质量的测定,题目难度中等,明确实验目的、实验原理为解答关键,是对学生综合能力的考查,需要学生具有扎实的基础与分析解决问题的能力.


 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 硬脂酸甘油酯在酸性条件下的水解反应叫皂化反应 | |
| B. | 淀粉和纤维素两者不是互为同分异构体,在一定条件下水解均可得到葡萄糖 | |
| C. | 蛋白质遇甲醛可发生变性而凝聚,遇伤口流血时,可在伤口处滴甲醛水溶液来止血 | |
| D. | 在乙酸与乙醛的混合溶液中加入银氨溶液,水浴加热,可观察到银镜现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的NaOH和KOH分别与足量的盐酸反应,前者消耗HCl的量比后者少 | |
| B. | 观察钠元素焰色反应的颜色要透过蓝色钴玻璃进行观察 | |
| C. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为2CaO•5MgO•8SiO2•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1 mol•L-1CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 在0.l mol•L-1的稀硫酸加水稀释的过程中,c(H+):c(SO42-)始终为2:1 | |
| C. | 向10 mL浓度为0.l mol•L-1CH3COOH溶液中滴加相同浓度的氨水至中性,在滴加过程中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$逐渐减小 | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)<c(SO42-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com