
ĻĀĮŠĒā»ÆĪļÖŠ£¬ĪČ¶ØŠŌ×īĒæµÄŹĒ £Ø £©
A£®HF B£®HCl C£®HBr D£®HI
 ŠĀĢāŠĶČ«³Ģ¼ģ²āĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
ŠĀĢāŠĶČ«³Ģ¼ģ²āĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ25”ꏱ£¬AgClµÄ°×É«Šü×ĒŅŗÖŠ£¬ŅĄ“Ī¼ÓČėµČÅØ¶ČµÄKIČÜŅŗŗĶNa2SČÜŅŗ”£¹Ū²ģµ½µÄĻÖĻóŹĒĻČ³öĻÖ»ĘÉ«³Įµķ£¬×īÖÕ³öĻÖŗŚÉ«³Įµķ”£ŅŃÖŖÓŠ¹ŲĪļÖŹµÄČܶȻżKsp (25”ę)ČēĻĀ£ŗ
| AgCl | AgI | Ag2S | |
| Ksp£Øµ„Ī»Ź”ĀŌ£© | 1.8”Į10-10 | 1.5”Į10-16 | 6.3”Į10-50 |
ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A£®³Įµķ×Ŗ»ÆµÄŹµÖŹ¾ĶŹĒ³ĮµķČܽāĘ½ŗāµÄŅʶÆ
B£®Čܽā¶ČŠ”µÄ³ĮµķČŻŅ××Ŗ»ÆĪŖČܽā¶ČøüŠ”µÄ³Įµķ
C£®AgCl¹ĢĢåŌŚµČĪļÖŹµÄĮæÅØ¶ČµÄNaCl”¢CaCl2ČÜŅŗÖŠµÄČܽā³Ģ¶ČĻąĶ¬
D£®25”ꏱ£¬ŌŚ±„ŗĶAgCl”¢AgI”¢Ag2SČÜŅŗÖŠ£¬Ėłŗ¬Ag+µÄÅØ¶Č²»Ķ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķس£×“æöĻĀ£¬NCl3ŹĒŅ»ÖÖÓĶדŅŗĢ壬Ęä·Ö×Óæռ乹ŠĶÓė°±·Ö×ÓĻąĖĘ£¬ĻĀĮŠ¶ŌNCl3µÄÓŠ¹Ų ŠšŹöÕżČ·µÄŹĒ(””””)
ŠšŹöÕżČ·µÄŹĒ(””””)
A£®NCl3·Ö ×ÓÖŠN—Cl¼üµÄ¼ü³¤±ČCCl4·Ö×ÓÖŠC—Cl¼üµÄ¼ü³¤³¤
×ÓÖŠN—Cl¼üµÄ¼ü³¤±ČCCl4·Ö×ÓÖŠC—Cl¼üµÄ¼ü³¤³¤
B£®NCl3·Ö×ÓŹĒ·Ē¼«ŠŌ·Ö×Ó
C£®·Ö×ÓÖŠµÄĖł ÓŠŌ×Ó¾ł“ļµ½8µē×ÓĪČ¶Ø½į¹¹
ÓŠŌ×Ó¾ł“ļµ½8µē×ÓĪČ¶Ø½į¹¹
D£®NBr3±ČNCl3Ņ×»Ó·¢
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
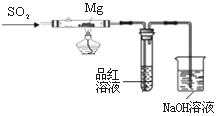 ijŠĖȤŠ”×éŅĄ¾ŻCO2+2Mg=2MgO+C£¬ĶĘ²āMgÓėSO2ŌŚøō¾ųæÕĘųĢõ¼žĻĀ·“Ó¦ŗó£¬Ź£Óą¹ĢĢåMæÉÄÜŗ¬ÓŠMgO”¢S”¢MgS”¢MgÖŠµÄŅ»ÖÖ»ņ¼øÖÖ”£ĪŖĮĖŃéÖ¤ĶĘ²ā£¬½ųŠŠŅŌĻĀŹµŃ锣Ēė»Ų“šÓŠ¹ŲĪŹĢā”£
ijŠĖȤŠ”×éŅĄ¾ŻCO2+2Mg=2MgO+C£¬ĶĘ²āMgÓėSO2ŌŚøō¾ųæÕĘųĢõ¼žĻĀ·“Ó¦ŗó£¬Ź£Óą¹ĢĢåMæÉÄÜŗ¬ÓŠMgO”¢S”¢MgS”¢MgÖŠµÄŅ»ÖÖ»ņ¼øÖÖ”£ĪŖĮĖŃéÖ¤ĶĘ²ā£¬½ųŠŠŅŌĻĀŹµŃ锣Ēė»Ų“šÓŠ¹ŲĪŹĢā”£
ŹµŃé¢ń °“ÓŅĶ¼ĖłŹ¾½ųŠŠŹµŃ锣
£Ø1£©ŹµŃéĒ°Šč³żČ„Ć¾Ģõ±ķĆęŃõ»ÆĤ”£ÓĆ¼ņŅ×µÄĪļĄķ
·½·Ø³żŃõ»ÆĤµÄ²Ł×÷ŹĒ £»
£Ø2£©ŹµŃéŹŅÖĘČ”¶žŃõ»ÆĮņµÄ»Æѧ·½³ĢŹ½ĪŖ £»
£Ø3£©ÉĻŹö×°ÖĆ“ęŌŚ²»ŗĻĄķÖ®“¦£¬ĒėĢį³ö1ĻīøĽų½ØŅé £»
 £Ø4£©ŹµŃ鏱£¬ĻČĶØČėSO2Ö±µ½ ĻÖĻó³öĻÖŗó£¬ŌŁµćČ¼¾Ę¾«µĘ£»“Ė²Ł×÷ÄæµÄŹĒ ”£
£Ø4£©ŹµŃ鏱£¬ĻČĶØČėSO2Ö±µ½ ĻÖĻó³öĻÖŗó£¬ŌŁµćČ¼¾Ę¾«µĘ£»“Ė²Ł×÷ÄæµÄŹĒ ”£
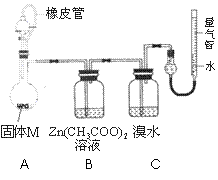
ŹµŃé¢ņ Č·¶Ø¹ĢĢåMµÄ³É·Ö”£
ŹµŃé×°ÖĆČēÓŅĶ¼ĖłŹ¾”£½«·ÖŅŗĀ©¶·ÖŠĻ”ĮņĖį£Ø×ćĮ棩
¼ÓČėµ½ÉÕĘæÖŠ£¬ĶźČ«·“Ó¦ŗó£¬ŹµŃéĻÖĻóČēĻĀ£ŗ
|
£Ø5£©ŹµŃ鏱£¬B×°ÖĆÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £»
£Ø6£©ŅŃÖŖĆ¾µÄĻą¶ŌŌ×ÓÖŹĮæĪŖ24£¬Ōņ¹ĢĢåMÖŠ½šŹōĆ¾µÄÖŹĮæĪŖ g£»ŹµŃéĒ°×°ÖĆÄŚÓŠæÕĘų£¬¶Ō½šŹōĆ¾ÖŹĮæµÄ²ā¶Ø½į¹ūµÄÓ°ĻģŹĒ £ØĢīĘ«µĶ”¢Ę«øß”¢ĪŽÓ°Ļģ£©£»
£Ø7£©ŅĄŅŌÉĻŹµŃ飬æÉČ·¶Ø¹ĢĢåMµÄ³É·ÖÓŠ ÖÖ£ØĢīŹż×Ö£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŌŖĖŲÖŠ£¬²»ŹōÓŚµŚ¢ńA×åµÄŹĒ£Ø £©
A£®ļ® B£®ÄĘ C£®Ć¾ D£®¼Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲŌ×Ó½į¹¹ŗĶŌŖĖŲÖÜĘŚĀɵıķŹöÕżČ·µÄŹĒ£Ø £©
¢ŁŌ×ÓŠņŹżĪŖ15µÄŌŖĖŲ×īøß»ÆŗĻ¼ŪĪŖ+3
¢ŚµŚVIIA×åŌŖĖŲŹĒĶ¬ÖÜĘŚÖŠ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲ
¢ŪµŚ¶žÖÜĘŚµŚIVA×åŌŖĖŲµÄŌ×ÓŗĖµēŗÉŹżŗĶÖŠ×ÓŹżŅ»¶ØĪŖ6
¢ÜŌ×ÓŠņŹżĪŖ12µÄŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚČżÖÜĘŚµŚ IIA×å
IIA×å
A£®¢Ł¢Ś B£®¢Ł¢Ū C£®¢Ś¢Ü D£®¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
SO2ŗĶCl2¾łŹĒ³£ÓƵÄĘÆ°×¼Į£¬Čō½«SO2ŗĶCl2µČĪļÖŹµÄĮæ»ģŗĻŗó£¬ĻČ»ŗĀżĶØČėµ½BaCl2ČÜŅŗÖŠ£¬ŌŁµĪČėĘ·ŗģŹŌŅŗ£¬»į¹Ū²ģµ½µÄĻÖĻóŹĒ£Ø £©
A. ĪŽ³ĮµķÉś³É£¬ČÜŅŗĻŌŗģÉ« B. ĪŽ³ĮµķÉś³É£¬ČÜŅŗĻŌĪŽÉ«
C. ÓŠ³ĮµķÉś³É£¬ČÜŅŗĻŌĪŽÉ« D. ÓŠ³ĮµķÉś³É£¬ČÜŅŗĻŌŗģÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻņCr2(SO4) 3µÄĖ®ČÜŅŗÖŠ£¬¼ÓČėNaOHČÜŅŗ£¬µ±pH=4.6Ź±£¬æŖŹ¼³öĻÖCr(OH)3³Įµķ£¬Ėę×ÅpHµÄÉżøߣ¬³ĮµķŌö¶ą£¬µ«µ±pH”Ż13Ź±£¬³ĮµķĻūŹ§£¬³öĻÖĮĮĀĢÉ«µÄŃĒøõĖįøłĄė×Ó£ØCrO2££©”£ĘäĘ½ŗā¹ŲĻµČēĻĀ£ŗ
Cr3++3OH£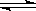 Cr(OH) 3””
Cr(OH) 3””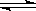 CrO2£+H++H2O
CrO2£+H++H2O
£Ø×ĻÉ«£© £Ø»ŅĀĢÉ«£© £ØĮĮĀĢÉ«£©
Ļņ0.05mol/LµÄCr2(SO4) 3ČÜŅŗ50mLÖŠ£¬¼ÓČė1.0mol/LµÄNaOHČÜŅŗ50mL£¬³ä·Ö·“Ó¦ŗó£¬ČÜŅŗÖŠæɹŪ²ģµ½µÄĻÖĻóĪŖ
A£®ČÜŅŗĪŖ×ĻÉ« B£®ČÜŅŗĪŖĮĮĀĢÉ«””””
C£®ČÜŅŗÖŠÓŠ»ŅĀĢÉ«³Įµķ D£®ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com