
某小组研究影响反应速率的因素。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c = mol·L-1。
编号 | 酸的种类 | 酸的浓度/mol·L-1 | 酸的体积/ml | 镁条质量/g |
1 | 醋酸 | 1.0 | 10 | 2.0 |
2 | 盐酸 | c | 10 | 2.0 |
②实验步骤:
(a)检查装置(左图)的气密性后,添加药品;
(b)反应开始后, ;
(c)将所记录的数据转化为曲线图(右图)。
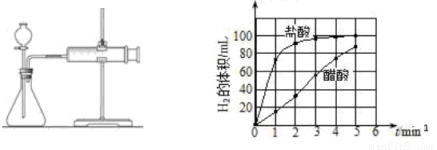
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律: 。
(2)实验二:探究反应条件对0.10mol/LNa2S2O3溶液与稀H2SO4反应速率的影响,其设计与测定结果如下:
编号 | 反应温度/℃ | Na2S2O3溶液/ml | V(蒸馏水)/ml | 0.10mol/LH2SO4溶液/ml | 乙 |
1 | 25℃ | 10.0 | 0 | 10.0 | |
2 | 25℃ | 5.0 | a | 10.0 | |
3 | 45℃ | 10.0 | 0 | 10.0 |
I.完成上述实验原理的离子方程式 。
II.上述实验1、3是探究 对化学反应速率的影响;若上述实验1、2是探究浓度对化学反应速率的影响,a为 ;乙是实验需要测量的物理量,则表格中“乙”应填写 。
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
下列溶液一定显酸性的是()
① pH<7的溶液 ② c(H+)=c(OH-)的溶液
③c(H+)=l×10-6mol/L的溶液 ④c(H+)>c(OH-)的溶液
⑤ 25℃下pH=6的溶液 ⑥能使酚酞试液显无色的溶液
A.①③④⑤⑥ B.②④⑤⑥ C.⑤⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
质子数和中子数之和为A,核内中子数为N的R2+离子与16O所形成的Wg氧化物中所含质子的物质的量为 ( )
A. mol B.
mol B. mol
mol
C.(A-N+8)mol D. mol
mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列说法正确的是

A.图①中△H2=△H1+△H3
B.图②在催化剂条件下,反应的活化能等于E1+E2
C.图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲 线
线
D.图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:选择题
下列有关阿伏加德罗常数NA说法正确的是
A.22 g 2H218O中含有的质子数为10NA
B.标准状况下,2.24 L乙醇中含有的C-H键数目为0.5NA
C.0.1 mol/L的NaF溶液中所含F﹣的数目小于0.1NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去0.5NA个电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:选择题
在一定温度下的恒容密闭容器中,当下列物理量不再发生变化时,无法表明反应:A(s)+3B(g) 2C(g)+D(g)已达平衡状态的是(仅B有颜色)
2C(g)+D(g)已达平衡状态的是(仅B有颜色)
A.混合气体的压强 B.混合气体的密度 C.气体的平均分子量 D.气体的颜色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:选择题
反应A+B→C(△t<0)分两步进行:① A+B→X (△H >0)② X→C(△H<0),下列示意图中,能正确表示总反应过程中能量变化的是

查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:填空题
(1)NaHCO3溶液中存在多种平衡关系,写出相应平衡关系所对应的离子方程式:_ _ 。
NaHCO3溶液显碱性的原因: _ 。
NaHSO4溶液显酸性的原因: 。
(2)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。放出571.6kJ的热量,表示H2燃烧热的热化学方程式为____________ 。
(3)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为______________ _ 。
(4)已知C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ/mol,
C(s)+0.5O2(g)=CO(g) △H3=akJ/mol,则a=__________
(5)已知N2(g) +3H2(g)  2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g)
2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g)  NH3(g) 的平衡常数为K2,NH3(g)
NH3(g) 的平衡常数为K2,NH3(g)  0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高一上第一次双周练化学卷(解析版) 题型:选择题
下列实验操作正确的是( )
A. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
B. 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下
C. 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D. 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com