
【题目】取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4:1)的混合气体;然后分别做溶解于水的喷泉实验.实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2:1:2
B.5:5:4
C.1:1:1
D.无法确定
【答案】B
【解析】解:假设烧瓶体积为5V,则干燥纯净的氨气体积为5V完全溶于水后烧瓶充满溶液溶液体积也是5V,溶质物质的量浓度为: ![]() =
= ![]() (mol/L); 含一半空气的氯化氢烧瓶中氯化氢体积为2.5V完全溶解后烧瓶进水
(mol/L); 含一半空气的氯化氢烧瓶中氯化氢体积为2.5V完全溶解后烧瓶进水 ![]() ,也就是溶液体积为2.5V,所以溶质物质的量浓度为:
,也就是溶液体积为2.5V,所以溶质物质的量浓度为: ![]() =
= ![]() (mol/L);
(mol/L);
二氧化氮与氧气体积比为 ![]() 的混合气中NO2体积为4V,
的混合气中NO2体积为4V,
根据以下方程式恰好完全反应:4NO2+O2+2H2O=4HNO3 , 而且生成硝酸物质的量为 ![]() (mol),
(mol),
由于完全反应所以烧瓶充满溶液其体积为5V,所以溶质的物质的量浓度为: ![]() =
= ![]() (mol/L).
(mol/L).
所以三个烧瓶中所得溶液的溶质的物质的量浓度之比为: ![]() (mol/L):
(mol/L): ![]() (mol/L):
(mol/L): ![]() (mol/L)=1:1:0.8=5:5:4,
(mol/L)=1:1:0.8=5:5:4,
故选B.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是可逆反应X2+3Y22Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( ) 
A.t1时,只有正方向反应
B.t2时,反应到达限度
C.t2﹣t3 , 反应不再发生
D.t2﹣t3 , 各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:
(1)A的分子式是C7H8 , 其结构简式是 .
(2)试剂a是 .
(3)反应③的化学方程式: .
(4)E的分子式是C6H10O2 . E中含有的官能团: .
(5)反应④的反应类型是 .
(6)反应⑤的化学方程式: .
(7)已知:2CH3CHO 
以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A.室温下,测得氯化铵溶液pH<7,证明一水合氨是碱:NH4++2H2O═NH3H2O+H3O+
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑
C.用碳酸氢钠溶液检验水杨酸中的羧基:  +2HCO3﹣→
+2HCO3﹣→  +2H2O+2CO2↑
+2H2O+2CO2↑
D.用高锰酸钾标准溶液滴定草酸:2MnO4﹣+16H++5C2O42﹣═2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Al、CuO、Fe2O3组成的混合物共10.0g,放入250mL某浓度的硫酸溶液中,混合物完全溶解,当再加入125mL 2.00mol/L的NaOH溶液时,得到沉淀物质的量最多.上述硫酸溶液的浓度为( )
A.0.500 mol/L
B.1.00 mol/L
C.2.00 mol/L
D.3.00 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)
(1)A、B、C、D代表的物质分别为、、、(填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是;
(3)反应②中,若B与F物质的量之比为4:3,G、H分别是、(填化学式);
(4)反应③产物中K的化学式为;
(5)反应④的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将14g铜银合金与足量某浓度的硝酸反应,使放出的气体与1.12L(标准状况)氧气混合恰好被水全部吸收生成硝酸,则合金中铜的质量为( )
A.3.2g
B.4.43g
C.10.8g
D.12.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质: A.O2和O3
B. ![]() C和
C和 ![]() C
C
C.CH3CH2CH2CH3和 ![]()
D. 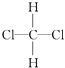 和
和 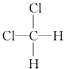
E.CH3CH2CH2CH3和 ![]()
(1)组两种物质属于同系物.
(2)组两种物质互为同素异形体.
(3)组两物质互为同分异构体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.二氧化锰和浓盐酸反应:MnO2+4HCl(浓) ![]() ?Mn2++2Cl2↑+2H2O
?Mn2++2Cl2↑+2H2O
B.稀盐酸和硅酸钠溶液反应:SiO32﹣+2H+═H2SiO3↓
C.碳酸钙和稀盐酸反应:CO32﹣+2H+═CO2↑+H2O
D.铜和氯化铁溶液反应:Fe3++Cu═Fe2++Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com