
把铁片分别放入下列物质的溶液中,充分反应后,溶液质量比反应前减轻的是
A.CuSO4 B.Fe2(SO4)3 C.HCl D.FeSO4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
对有机物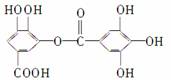 ,叙述不正确的是( )
,叙述不正确的是( )
A.常温下,与Na2CO3溶液反应放出CO2
B.能发生碱性水解,1 mol该有机物能消耗8 mol NaOH
C.与稀H2SO4共热生成两种有机物
D.该有机物的分子式为C14H10O9
查看答案和解析>>
科目:高中化学 来源: 题型:
)已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体, C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
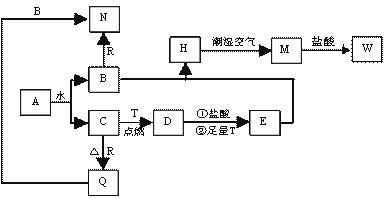
(1)写出下列物质的化学式:
A: D: R: 。
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式: ;
向N中通足量CO2时反应的离子方程式: ;
D与盐酸反应的离子方程式: 。
(3)简述检验气体C的方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为
3FeS2+8O2===6SO2+Fe3O4,氧化产物为 ,若有3mol FeS2参加反应,转移
mol电子.
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为
(用离子方程表示)
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请写出相应的离子方程式:
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL 5mol•L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为
查看答案和解析>>
科目:高中化学 来源: 题型:
新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度低于570℃时反应的化学方程式 。
(2)中学教材中用右图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是
。
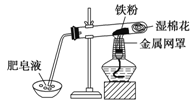
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图发生该反应并有氢气的收集装置图(包括反应时容器中的物质)。
 |
说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽:
 试管:
试管:
 蒸发皿:
蒸发皿:
 玻璃导管:
玻璃导管:
 或
或
 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)乙同学为了探究实验后的固体产物是否存在Fe3O4(假定铁全部反应完全)设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液X中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2符合 关系时,才能确定固体样品中一定只存在Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
橄榄石型LiFePO4是以中国锂离子电池正极材料,下列有关LiFePO4的说法中不正确的是
A. LiFePO4中铁元素的化合价为+2价
B. LiFePO4中Li、P、O均属于短周期元素
C. 能与稀硝酸发生氧化还原反应
D. LiFePO4中Li、Fe、P均属于主族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
、将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g.则下列叙述中不正确的是( )
A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL
B.当金属全部溶解时收集到NO气体的体积一定为2.24L
C.参加反应的金属的总质量为9.6g>m>3.6g
D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列相关的离子方程式书写正确的是
A.NaHS溶液水解: HS- + H2O 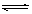 S2- + H3O+
S2- + H3O+
B.向Ca(C1O)2溶液中通入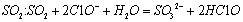
C.硫酸与氢氧化钡溶液混合: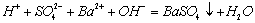
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42ˉ刚好沉淀完全:
Ba2+ + 2OH- + NH4+ + H+ + SO42- = BaSO4↓+ NH3·H2O + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com