
| »ÆѧŹ½ | CH3COOH | H2CO3 | HClO |
| µēĄėĘ½ŗā³£Źż | 1.7”Į10-5 | K1=4.3”Į10-7 K2=5.6”Į10-11 | 3.0”Į10-8 |
·ÖĪö £Ø1£©ĖįŠŌŌ½Ē棬ĘäĖįøłĄė×ÓµÄĖ®½āÄÜĮ¦Ō½Čõ£¬¶ŌÓ¦ČÜŅŗµÄpHŌ½Š”£»
£Ø2£©Ö¤Ć÷ŃĪĖįµÄĖįŠŌ±Č“×ĖįµÄĖįŠŌĒæµÄ·½·ØÓŠ£ŗ²ā¶ØĻąĶ¬ÅØ¶Č“×ĖįŗĶŃĪĖįČÜŅŗµÄPHÖµ“󊔣»ÓĆĻąĶ¬ÅØ¶ČµÄŃĪĖįŗĶ“×Ėį·Ö±šŗĶĢ¼ĖįøĘ·“Ó¦£¬øł¾Ż·“Ó¦ĖŁĀŹÅŠ¶Ļ£»Ķعż±Č½ĻĢå»żĻąĶ¬”¢pHĻąĶ¬µÄĖįČÜŅŗĶ¬±¶ŹżĻ”ŹĶŗó£¬ČÜŅŗµÄpH±ä»Æ“󊔥“¼ų±šµČ£®
½ā“š ½ā£ŗ£Ø1£©ĖįŠŌŌ½Ē棬ĘäĖįøłĄė×ÓµÄĖ®½āÄÜĮ¦Ō½Čõ£¬¶ŌÓ¦ČÜŅŗµÄpHŌ½Š”£¬ĖįŠŌ£ŗCH3COOH£¾H2CO3£¾HClO£¾HCO3-£¬ŌņĖįøłĄė×ÓµÄĖ®½āÄÜĮ¦£ŗCO32-£¾ClO-£¾HCO3-£¾CH3COO-£¬ŌņČÜŅŗµÄpHÓɓ󵽊”µÄĖ³ŠņŹĒ£ŗ¢Ū£¾¢Ü£¾¢Ś£¾¢Ł£¬¹Ź“š°øĪŖ£ŗ£ŗ¢Ū£¾¢Ü£¾¢Ś£¾¢Ł£»
£Ø2£©Ö¤Ć÷ŃĪĖįµÄĖįŠŌ±Č“×ĖįµÄĖįŠŌĒæµÄ·½·ØÓŠ£ŗ²ā¶ØĻąĶ¬ÅØ¶Č“×ĖįŗĶŃĪĖįČÜŅŗµÄPHÖµ“󊔣»ÓĆĻąĶ¬ÅØ¶ČµÄŃĪĖįŗĶ“×Ėį·Ö±šŗĶĢ¼ĖįøĘ·“Ó¦£¬øł¾Ż·“Ó¦ĖŁĀŹÅŠ¶Ļ£»Ķعż±Č½ĻĢå»żĻąĶ¬”¢pHĻąĶ¬µÄĖįČÜŅŗĶ¬±¶ŹżĻ”ŹĶŗó£¬ČÜŅŗµÄpH±ä»Æ“󊔥“¼ų±šµČ£®
A£®ÓĆPH¼Ę²ā¶ØµČÅØ¶ČµÄĮ½ÖÖČÜŅŗµÄPH£¬²ā¶ØČÜŅŗPHŠ”µÄĪŖŃĪĖį£¬¹ŹAÕżČ·£»
B£®½«PH=3µÄĮ½ČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶ100±¶ŗó£¬ŌŁÓĆPH¼Ę²ā¶ØČÜŅŗµÄPH£¬PH±ä»Æ“óµÄĪŖŃĪĖį£¬¹ŹBÕżČ·£»
C£®Č”ÅØ¶Č¾łĪŖ0.1mol/LµČĢå»żµÄĮ½ČÜŅŗ·Ö±šµĪ¼Ó0.1mol/LµÄĒāŃõ»ÆÄĘČÜŅŗÖĮĒ”ŗĆĶźČ«ÖŠŗĶ£¬²ā¶ØĻūŗÄĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĻąĶ¬£¬²»ÄÜĖµĆ÷ĖįŠŌĒæČõ£¬¹ŹC“ķĪó£»
D£®²ā¶ØPH=3µÄĮ½ČÜŅŗµÄµ¼µēŠŌ£¬ČÜŅŗÖŠĄė×ÓÅضČĻąĶ¬£¬µ¼µēŠŌĻąĶ¬£¬²»ÄÜĖµĆ÷ĖįŠŌĒæČõ£¬¹ŹD“ķĪó£»
E£®ÓĆPHŹŌÖ½²ā¶ØµČÅØ¶ČµÄNaClČÜŅŗŗĶCH3COONaČÜŅŗµÄĖį¼īŠŌ£¬ČōĻŌ¼īŠŌÖ¤Ć÷“×ĖįÄĘČÜŅŗÖŠ“×ĖįøłĄė×ÓĖ®½ā£¬Ö¤Ć÷“×ĖįĪŖČõĖį£¬ĀČ»ÆÄĘČÜŅŗ³ŹÖŠŠŌĪŖĒæĖįĒæ¼īŃĪ£¬¹Ź“š°øĪŖ£ŗA”¢B”¢E£»
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµēĄėĘ½ŗā”¢ŃĪĄąĖ®½āÓ¦ÓĆ”¢Čõµē½āÖŹµÄŃéÖ¤·ÖĪöÅŠ¶Ļ£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L0.1 mol•L-1ŃĪĖįŗĶ1L mol•L-1ĮņĖį·Ö±šÓė1 L2 mol•L-1NaOHČÜŅŗ·“Ó¦ĖŁĀŹĻąĶ¬ | |
| B£® | »Æѧ·“Ó¦ĖŁĀŹĪŖ0.8 mol•L-1•s-1£¬Ęäŗ¬ŅåŹĒŹ±¼äĪŖ1sŹ±£¬Ä³ĪļÖŹµÄÅØ¶ČŹĒ0.8mol•L-1 | |
| C£® | 0.1 mol•L-1ĻõĖįÓėĻąĶ¬ŠĪדŗĶ“󊔵ēóĄķŹÆ·“Ó¦µÄĖŁĀŹĻąĶ¬ | |
| D£® | ¶ŌÓŚČĪŗĪ»Æѧ·“Ó¦Ą“Ėµ£¬·“Ó¦ĖŁĀŹŌ½“󣬷“Ó¦ĻÖĻó¾ĶŌ½Ć÷ĻŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Įņ¼°Ęä»ÆŗĻĪļ¶ŌČĖĄąµÄÉś²śŗĶÉś»īÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ£®
Įņ¼°Ęä»ÆŗĻĪļ¶ŌČĖĄąµÄÉś²śŗĶÉś»īÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ£®| ŹµŃé ±ąŗÅ | ĪĀ¶Č | ĘšŹ¼Ź±ĪļÖŹµÄĮæ/mol | Ę½ŗāŹ±ĪļÖŹµÄĮæ/mol | |
| n£ØSO2£© | n£ØNO2£© | n£ØNO£© | ||
| ¼× | T1 | 0.80 | 0.20 | 0.18 |
| ŅŅ | T2 | 0.20 | 0.80 | 0.16 |
| ±ū | T2 | 0.20 | 0.30 | a |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
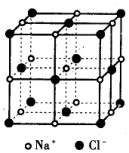 ŅŃÖŖNaClµÄĦ¶ūÖŹĮæĪŖ58.5g•mol-1£¬Ź³ŃĪ¾§ĢåµÄĆܶČĪŖ¦Ńg•cm-3£¬ČōĶ¼ÖŠNa+Óė×īĮŚ½üµÄCl-µÄŗĖ¼ä¾ąĄėĪŖa cm£¬ÄĒĆ“°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµæɱķŹ¾ĪŖ£Ø””””£©
ŅŃÖŖNaClµÄĦ¶ūÖŹĮæĪŖ58.5g•mol-1£¬Ź³ŃĪ¾§ĢåµÄĆܶČĪŖ¦Ńg•cm-3£¬ČōĶ¼ÖŠNa+Óė×īĮŚ½üµÄCl-µÄŗĖ¼ä¾ąĄėĪŖa cm£¬ÄĒĆ“°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµæɱķŹ¾ĪŖ£Ø””””£©| A£® | 117¦Į3¦Ń | B£® | $\frac{M}{N{¦Į}^{3}}$ | C£® | $\frac{234}{{¦Į}^{3}¦Ń}$ | D£® | $\frac{58.5}{2{¦Į}^{3}¦Ń}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ü | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol Al3+ŗ¬ÓŠµÄŗĖĶāµē×ÓŹżĪŖ3NA | |
| B£® | ½«5.85 g NaClČÜÓŚ100gĖ®ÖŠ£¬ĖłµĆNaClČÜŅŗµÄÅضČĪŖ1.00mol•L-1 | |
| C£® | 1 mol Cl2Óė×ćĮæµÄĢś·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA | |
| D£® | ³£ĪĀĻĀ£¬pH=1µÄĮņĖįČÜŅŗÖŠŗ¬ÓŠµÄH+ŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4·Ö×ӵıȥżÄ£ŠĶ£ŗ | B£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CH2 | ||
| C£® | Ō×ÓŗĖÄŚÓŠ10øöÖŠ×ÓµÄŃõŌ×Ó£ŗ18O | D£® | CO2µÄĢī³äÄ£ŠĶ£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³äµēŹ±£¬·“Ó¦ĆæÉś³É1mol H+Ź±µē×Ó×ŖŅʵÄĪļÖŹµÄĮæĪŖ1mol | |
| B£® | ·Åµē¹ż³ĢÖŠ£¬Õż¼«ø½½üČÜŅŗµÄĖįŠŌ¼õČõ | |
| C£® | ·ÅµēŹ±£¬Õż¼«·“Ó¦ĪŖVO2++2H++e-ØTVO2++H2O | |
| D£® | ³äµēŹ±£¬Ņõ¼«ø½½üČÜŅŗÓÉ×ĻÉ«Öš½„±äĪŖĀĢÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ĢåÓż¾ŗ¼¼ÖŠ·žÓĆŠĖ·Ü¼Į¼ČÓŠŹ§¹«Ę½£¬Ņ²°Ü»µĮĖĢåÓżµĄµĀ£®Ä³ÖÖŠĖ·Ü¼ĮµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
ĢåÓż¾ŗ¼¼ÖŠ·žÓĆŠĖ·Ü¼Į¼ČÓŠŹ§¹«Ę½£¬Ņ²°Ü»µĮĖĢåÓżµĄµĀ£®Ä³ÖÖŠĖ·Ü¼ĮµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆĪļÖŹ·Ö×ÓŹ½ĪŖC17H20O4 | |
| B£® | øĆĪļÖŹæÉŅŌ·¢ÉśŃõ»Æ·“Ó¦”¢õ„»Æ·“Ó¦ŗĶĻūČ„·“Ó¦ | |
| C£® | 1moløĆĪļÖŹ·Ö±šÓėÅØäåĖ®ŗĶH2·“Ó¦Ź±×ī¶ąĻūŗÄBr2ŗĶH2·Ö±šĪŖ4molŗĶ7mol | |
| D£® | øĆĪļÖŹÓŠĖįŠŌ£¬1moløĆĪļÖŹÓėNaOH·“Ó¦Ź±×ī¶ąĻūŗÄNaOHĪŖ3mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com