
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
(1)写出CO2和Na2O2反应的化学方程式: 。
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗? 。简要说明理由: 。
(3)该同学无法断定SO2和Na2O2反应中是否有氧气生成,拟使用下列装置进行实验。
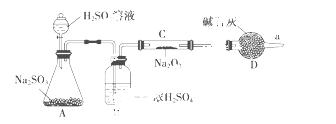
装置中B的作用是 ,
D的作用是 。
(4)为确认SO2和Na2O2的反应产物,该同学设计了以下实验步骤:你认为应进行的操作按顺 序排列是(填序号) 。
序排列是(填序号) 。
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧
B.将C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液, 观察是否有沉淀生
观察是否有沉淀生 成
成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
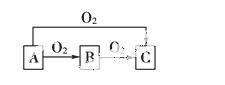 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):
(1)若A是一种金属,C是淡黄色固体,则B的化学式为________,A→C反应的化学方程式为______________________。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为________,B→C反应的化学方程式为__________________。
A和C是否可以反应________,若能,写出反应的化学方程式,若不能,此空不填______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将15 mL 2 mol·L-1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1 MCln盐溶液中,恰好将溶液中的Mn+完全沉淀为碳酸盐,则盐MCln中n值是( )
A.4 B.3 C.2 D.1
查看答案和解析>>
科目:高中化学 来源: 题型:
有关碱金属的叙述正确的是 ( )
A.随核电荷数的增加,碱金属单质的熔点逐渐降 低,密度逐渐增大
低,密度逐渐增大
B.碱金属单质的金属性很强,均易与氯气、氧气、氮气等发生反应
C.碳酸铯加热时不能分解为二氧化碳和氧化铯
D.无水硫酸铯的化学式为Cs2SO4,它不易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后 者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是 ( )
者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是 ( )
A.2.0 mol·L-1 B.1.5 mol·L-1
C.0.18 mol·L-1 D.0.24 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中,溶液里无固体析出的是( )
A.MgCl2溶液中加入Na的小颗粒
B.Ca(OH)2饱和溶液中加入Na的小颗粒
C.KNO3稀溶液中加入Na的小颗粒
D.水中加入Na的小颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种化合物均含有同一种短周期常见金属元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E易溶于水。若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片)。
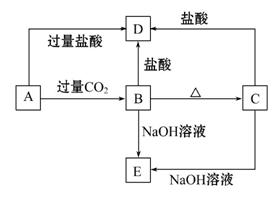
(1)写出化学式:A ,B ,C ,
D ,E 。
(2)写出下列反应的离子方程式:
A→B: _________________________________。
A→D: ________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为充分利用海洋资源,研究人员发明海水电池,这
种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表 示为:
示为:
5MnO2+2Ag+2NaCl=Na2 Mn5O10+2AgCl
Mn5O10+2AgCl
下列说法错误的是
A.负极反应式: Ag+Cl——e-=AgCl B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Cl—不断向电池的正极移动 D.Na2Mn5O10是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com