
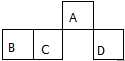
 短周期元素A、B、C、D在元素周期表中的相对位置如图.其中A原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素A、B、C、D在元素周期表中的相对位置如图.其中A原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:rD>rC>rB>rA | |
| B. | 含D元素的盐溶液一定显中性 | |
| C. | 氢化物的热稳定性:C>D | |
| D. | D的单质能与A形成的氢化物反应生成具有漂白性的物质 |
分析 由短周期元素在周期表中的位置可知,A处于第二周期,B、C、D处于第三周期,A原子的最外层电子数是最内层电子数的3倍,最外层电子数为6,则A为O,可推知B为Si,C为P,D为Cl.
A.同周期随原子序数增大原子半径减小,一般电子层越多原子半径越大;
B.NaCl溶液呈中性,NaClO溶液呈碱性;
C.非金属性越强,对应氢化物越稳定;
D.氯气与水反应生成HCl与HClO,HClO具有漂白性.
解答 解:由短周期元素在周期表中的位置可知,A处于第二周期,B、C、D处于第三周期,A原子的最外层电子数是最内层电子数的3倍,最外层电子数为6,则A为O,可推知B为Si,C为P,D为Cl.
A.同周期随原子序数增大原子半径减小,一般电子层越多原子半径越大,则原子半径为rB>rC>rD>rA,故A错误;
B.D为Cl,NaCl溶液呈中性,NaClO溶液呈碱性,故B错误;
C.非金属性D(Cl)>C(P),则最简单气态氢化物的热稳定性为D>C,故C错误;
D.氯气与水反应生成HCl与HClO,HClO具有漂白性,故D正确,
故选D.
点评 本题考查结构性质位置关系应用,A为推断的突破口,熟练掌握元素周期律与元素化合物性质,题目难度中等.


科目:高中化学 来源: 题型:填空题
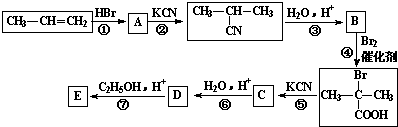
 ;
; +2C2H5OH$?_{△}^{浓硫酸}$
+2C2H5OH$?_{△}^{浓硫酸}$ +2H2O.
+2H2O. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | -3、+5 | -2 |
| A. | X、Y元素的金属性:X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以和Z的氢化物反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、Cl-、NO3-等离子能在甲基橙试液显红色的溶液中共存 | |
| B. | K+、Mg2+、Cl-、I-等离子能在[H+]=10-12 mol•L-1的溶液中共存 | |
| C. | NaHS水解的离子方程式为:HS-+H2O?S2-+H3O+ | |
| D. | NaHCO3的电离方程式为:NaHCO3=Na++HCO3-,HCO3-?H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
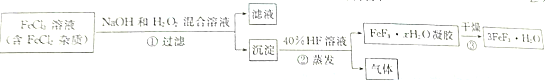
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| B | ||
| F |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为60% | |
| B. | 在25℃时,反应可表示为X+3Y═2Z,其平衡常数为1600 | |
| C. | 增大压强使平衡向生成Z的方向移动,平衡常数增大 | |
| D. | 升高温度此反应的平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电 | |
| B. | 一束可见光透过胶体时,有丁达尔效应产生 | |
| C. | 胶体属于混合物 | |
| D. | 氢氧化铁胶体能吸附水中的悬浮颗粒并沉淀,因此常用于净水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com