
分析 电解CuSO4溶液,先在A上收集到5.6L即0.25mol气体,即为氧气,发生反应:4OH--4e-=2H2O+O2↑;A是阳极,B极上发生反应:Cu2++2e-=Cu,该电极析出金属铜,B是阴极,根据电子守恒计算生成金属铜的物质的量,然后电极反接,在B极上收集到5.6L气体即为氧气,此时B是阳极,先是金属铜失电子,然后是4OH--4e-=2H2O+O2↑,根据电子守恒计算即可.
解答 解:电解CuSO4溶液,先在A上收集到5.6L即0.25mol气体,即为氧气,发生反应:4OH--4e-=2H2O+O2↑;此时转移电子1mol,A是阳极,B极上发生反应:Cu2++2e-=Cu,该电极析出金属铜,B是阴极,根据电子守恒,转移1mol电子,生成金属铜的物质的量是0.5mol,然后电极反接,在B极上收集到5.6L气体即为氧气,此时B是阳极,先是金属铜失电子,发生反应:Cu-2e-=Cu2+,转移电子1mol,然后是4OH--4e-=2H2O+O2↑,收集到5.6L0.25mol气体转移电子1mol,所以转移电子是2mol,
故答案为:2.
点评 本题考查电解的计算,主要考查学生的分析能力,根据电极反接先后发生的电极反应是解题的关键.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:填空题
| 周期数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H14+9O2→CO+5CO2+7H2O | B. | C6H14+7O2→5CO+CO2+7H2O | ||
| C. | C6H14+8O2→3CO+3CO2+7H2O | D. | 2C6H14+15O2→8CO+4CO2+14H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
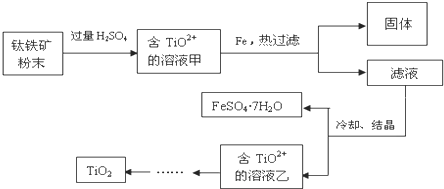
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KSP(AB2)小于KSP(CD),则AB2的溶解度一定小于CD的溶解度 | |
| B. | 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大 | |
| C. | 在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 | |
| D. | 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难溶电解质沉淀的速率和溶解的速率相等 | |
| B. | 溶液中各离子的浓度不再改变 | |
| C. | 难溶电解质在水中形成饱和溶液 | |
| D. | 加水可使难溶电解质的KSP增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V3>V2>V1 | B. | V1=V2=V3 | C. | V2>V1=V3 | D. | V1=V2<V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 苯、溴水和铁屑混合于带长导管的烧瓶中 | 制备溴苯 |
| B | 淀粉溶液水解后冷却至室温,加碘水观察现象 | 检验淀粉是否完全水解 |
| C | 向蔗糖溶液中加入适量稀硫酸,水浴加热,再加入新制的Cu(OH)2,加热至沸腾 | 检验蔗糖水解产物 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com