
| A. | 做银镜反应后的试管用氨水洗涤 | |
| B. | 苯酚如不慎沾到皮肤上,应立即用酒精洗涤 | |
| C. | 乙酸乙酯与稀硫酸混合水浴加热,酯层完全消失 | |
| D. | 向2mL10%硫酸铜溶液滴加4~6滴2%氢氧化钠溶液中,再加入0.5mL乙醛溶液加热,有红色沉淀出现 |
分析 A、银单质与氨水不反应;
B、苯酚易用于酒精;
C、酯类在酸性条件下的水解是可逆反应;
D、配制氢氧化铜悬浊液时,使用的氢氧化钠溶液必须过量.
解答 解:A、银单质与氨水不反应,可用稀硝酸洗去,故A错误;
B、苯酚有毒,且苯酚易用于酒精,故可以用酒精洗去沾在皮肤上的苯酚,故B正确;
C、酯类在酸性条件下的水解是可逆反应,不能水解彻底,故酯类不能完全消失,故C错误;
D、配制氢氧化铜悬浊液时,使用的氢氧化钠溶液必须过量,而向2mL10%硫酸铜溶液滴加4~6滴2%氢氧化钠溶液,NaOH的量不足,故加入乙醛溶液,实验会失败,不会有红色沉淀出现,故D错误.
故选B.
点评 本题考查化学实验基本操作和实验危险的处理以及实验操作的要点,难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
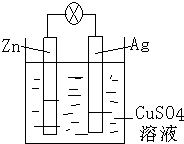 化学反应与能量有着密不可分的关系,回答下列问题.
化学反应与能量有着密不可分的关系,回答下列问题.| 物质 | H2 | CO | CH4 |
| 燃烧热(kJ•mol-1) | 285.8 | 283.0 | 890.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈橙红色 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
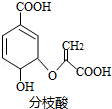
| A. | 可与乙醇、乙酸反应,且反应类型相同 | |
| B. | 分子中含有3种官能团 | |
| C. | 1mol分枝酸最多可与3molNaOH发生中和反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2、SO2均是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 二氧化硫有漂白性,通入少量紫色石蕊试液中,充分振荡后溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液:c (SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| B. | 常温下pH=2的HCl溶液与pH=12的氨水溶液等体积混合c(NH4+)=c(Cl-) | |
| C. | 0.2 mol•L-1 Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 某二元弱酸的酸式盐NaHA溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com