
��14�֣�I��ú̿����FeS2��ʽ���ڵ�������ˮ�Ϳ�������������������·�������������ԭ��Ӧ���йط�Ӧ�����ӷ���ʽ����Ϊ��
��2FeS2+7O2+2H2O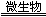 4H++2Fe2++4SO42- �� ��Fe2++O2+H+
4H++2Fe2++4SO42- �� ��Fe2++O2+H+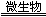 Fe3++____________��
Fe3++____________��
��FeS2+2Fe3+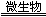 3Fe2++2S�� ��2S+3O2+2H2O
3Fe2++2S�� ��2S+3O2+2H2O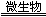 4H++2SO42����
4H++2SO42����
��֪��FeS2�е���Ԫ��Ϊ��1�ۡ�
�ش��������⣺
��1�����������غ㶨�ɺ͵���غ㶨�ɣ������������ӷ���ʽ��ƽ������������
��2����Ӧ�۵Ļ�ԭ����__________________��
��3���۲�������Ӧ����Ԫ������ת��Ϊ____________��ú̿�з������
II���ڵ���KI��Һ�У���������NaClO��Һ����Һ�����������йط�Ӧ�����ӷ���ʽ��___________�� ��������ɫ��Һ�У������μ�������NaClO��Һ����ɫ����ʧ���йط�Ӧ�����ӷ���ʽ��___________������ʾ����Ԫ�ر�������IO3����������ʵ���֪��ClO����I2��IO3������������ǿ������˳���� ��
III����ҵ���û�ͭ�� CuFeS2��ұ��ͭ������Ʒ��Ҳ��SO2 ��ұ��ͭ�ķ�ӦΪ8CuFeS2+ 21O2  8Cu+4FeO+2Fe2O3+16SO2.��CuFeS2�� Fe �Ļ��ϼ�Ϊ��2 ����Ӧ�б���ԭ��Ԫ���� ����Ԫ�ط��ţ���������0.8 molͭʱ���˷�Ӧת�Ƶĵ�����Ŀ��___________________��
8Cu+4FeO+2Fe2O3+16SO2.��CuFeS2�� Fe �Ļ��ϼ�Ϊ��2 ����Ӧ�б���ԭ��Ԫ���� ����Ԫ�ط��ţ���������0.8 molͭʱ���˷�Ӧת�Ƶĵ�����Ŀ��___________________��
I����1��4��1��4��4 ��2H2O��2�֣�����2��FeS2; ��1�֣���3��������
II��2I-+ClO-+H2O=I2+Cl-+2OH-��2�֣���I2+5ClO-+2OH-=2IO3-+5Cl -+H2O(2��)��ClO-> IO3-> I2��
III��Cu��O(2��)��10NA(2��)
��������
�����������1�����������غ㶨�ɺ͵���غ㶨�ɣ����������ӷ���ʽ��4Fe2++O2+4H+ 4Fe3++2H2O����2���ڷ�Ӧ�۵Ļ�ԭ����FeS2����3��ͨ���۲����������Ӧ��֪����Ԫ������ת��Ϊ�����δ�ú̿�з��������II���ڵ���KI��Һ�У���������NaClO��Һ����Һ�������������������غ㶨�ɼ�����غ㼰�����غ㣬��÷�Ӧ�����ӷ���ʽ��2I-+ClO-+H2O=I2+Cl-+2OH-����������ɫ��Һ�У������μ�������NaClO��Һ��I2���������ɫ����ʧ���йط�Ӧ�����ӷ���ʽ��I2+5ClO-+2OH-=2IO3-+5Cl -+H2O�����������ԣ�������>����������������ԣ�ClO-> I2; ClO-> IO3-,����ͬһԪ����˵��һ����Ԫ�صĻ��ϼ�Խ�ߣ�������������Ծ�Խǿ�����������ԣ�IO3-> I2;��ClO����I2��IO3������������ǿ������˳����ClO-> IO3-> I2��III. �ڷ�Ӧ��8CuFeS2+ 21O2
4Fe3++2H2O����2���ڷ�Ӧ�۵Ļ�ԭ����FeS2����3��ͨ���۲����������Ӧ��֪����Ԫ������ת��Ϊ�����δ�ú̿�з��������II���ڵ���KI��Һ�У���������NaClO��Һ����Һ�������������������غ㶨�ɼ�����غ㼰�����غ㣬��÷�Ӧ�����ӷ���ʽ��2I-+ClO-+H2O=I2+Cl-+2OH-����������ɫ��Һ�У������μ�������NaClO��Һ��I2���������ɫ����ʧ���йط�Ӧ�����ӷ���ʽ��I2+5ClO-+2OH-=2IO3-+5Cl -+H2O�����������ԣ�������>����������������ԣ�ClO-> I2; ClO-> IO3-,����ͬһԪ����˵��һ����Ԫ�صĻ��ϼ�Խ�ߣ�������������Ծ�Խǿ�����������ԣ�IO3-> I2;��ClO����I2��IO3������������ǿ������˳����ClO-> IO3-> I2��III. �ڷ�Ӧ��8CuFeS2+ 21O2  8Cu+4FeO+2Fe2O3+16SO2. CuFeS2��Fe �Ļ��ϼ�Ϊ��2����Ӧ������ΪFe2O3��S�ڷ�Ӧǰ���ϼ��ǣ�2�ۣ���Ӧ������Ϊ+4�۵�SO2��Cu��+2�ۣ�O2��OԪ�صĻ��ϼ���0�ۣ���Ӧ��ԭ��Ϊ��2�ۣ����Է�Ӧ��ԭΪ0�ۣ�����Ӧ�б���ԭ��Ԫ����Cu��O�����ݷ�Ӧ����ʽ��֪��ÿ����8mol��Cu,ת�Ƶ���100mol�����Ե�����0.8 molͭʱ���˷�Ӧת�Ƶĵ�����Ŀ��10NA��
8Cu+4FeO+2Fe2O3+16SO2. CuFeS2��Fe �Ļ��ϼ�Ϊ��2����Ӧ������ΪFe2O3��S�ڷ�Ӧǰ���ϼ��ǣ�2�ۣ���Ӧ������Ϊ+4�۵�SO2��Cu��+2�ۣ�O2��OԪ�صĻ��ϼ���0�ۣ���Ӧ��ԭ��Ϊ��2�ۣ����Է�Ӧ��ԭΪ0�ۣ�����Ӧ�б���ԭ��Ԫ����Cu��O�����ݷ�Ӧ����ʽ��֪��ÿ����8mol��Cu,ת�Ƶ���100mol�����Ե�����0.8 molͭʱ���˷�Ӧת�Ƶĵ�����Ŀ��10NA��
���㣺����������ԭ��Ӧ���й�֪ʶ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵڶ����¿�������ѧ�Ծ��������棩 ���ͣ������
��12�֣�A��B��C��X��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ������������ȥ����
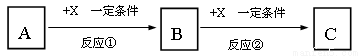
�Իش�
��1����X��ǿ�����Ե��ʣ���A��������________________��
A S B N2 C Na D��Mg E��Al
��2����X�ǽ������ʣ���C��ˮ��Һ�еμ�AgNO3��Һ������������ϡHNO3�İ�ɫ��������B�Ļ�ѧʽΪ_________��C��Һ������ʱӦ��������X��������________________________�����ñ�Ҫ�����ֺ����ӷ���ʽ��ʾ�������C��Һ�н���Ԫ�ؼ�̬�IJ���������____________________________��
��3����A��B��CΪ���н���Ԫ�ص��������XΪǿ���ǿ�A��Һ��C��Һ��Ӧ����B����Ӧ�ٵ����ӷ���ʽ����Ϊ____ ___________��____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ���и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��36.5����Ũ����(�ܶ�1.2 g��cm��3)��1 mol��L��1��ϡ���� 100 mL�����ƹ������õ���Щ���������Ⱥ�˳����ȷ���Ǣ�100 mL��Ͳ ��10 mL��Ͳ ��50 mL �ձ� ��������ƽ ��100 mL����ƿ��ͷ�ι� �߲�����
A���٢ۢݢޢ� B���ڢۢߢݢ� C���ۢݢߢޢ� D���ܢۢߢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ�ѡ����
����˵����ȷ����
A��HClO����Ԫ�ػ��ϼ۱�HClO4����Ԫ�ػ��ϼ۵ͣ����ԣ�HClO4��������ǿ
B����֪��Fe + Cu2+ = Fe2+ + Cu���� 2Fe3+ + Cu = 2Fe2+ + Cu2+����������ǿ��˳��Ϊ��Fe3+ > Cu2�� > Fe2+
C����֪��ԭ�ԣ�B�� > C��> D������Ӧ 2C�� + D2 = 2D�� +C2�ͷ�Ӧ 2C��+ B2=2B��+C2���ܷ���
D������ǿ�����Ժ�ǿ��ԭ�Ե����ʷ���һ����ܷ���������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ�ѡ����
���жԻ�ѧ֪ʶ������������
A�����������ﶼ�Ƿǽ���������
B��һ��Ԫ�ؿ����ж����������ͬ�ֻ��ϼ�ֻ��Ӧһ��������
C�������ЧӦ������������Һ�뽺�壬�ơ������ܲ��������ЧӦ
D������״̬�ܵ��������һ�������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵ�һ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��������ʵ�������ȷ���� ( )
A��Ư����Һ�ڿ�����ʧЧ��ClO����CO2��H2O =HClO��HCO3-
B����Ũ������MnO2��Ӧ��ȡ���������� MnO2��2H����2Cl�� 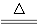 Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
C����С�մ�����θ����ࣺHCO3-+H+=CO2��+H2O
D����ǿ����Һ�д���������Fe(OH)3��Ӧ����Na2FeO4��
3ClO����2Fe(OH)3 =2FeO42-��3Cl����H2O��4H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵ�һ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݡ��ݴ�����˵����ȷ���ǣ� ��

A�����Լ������ʵ���Ũ��Ϊ9.2 mol��L��1
B��������50 mL��������ͭ��Ӧ�ɵõ���״����SO2 10.3 L
C������200 mL 4.6 mol��L��1��ϡ������ȡ������50 mL
D����������������ˮ���������Һ����������С��49%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�ij��и�����ѧ�ڵ�һ�ν��Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ����±���
Ԫ�ش��� | X | Y | Z | M | R |
ԭ�Ӱ뾶/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
��Ҫ���ϼ� | ��1 | ��6 ��2 | ��5 ��3 | ��2 | ��3 |
��֪X�Ƕ�����������õĽ���������Rͬ���ڡ�������������ȷ���� ( )
A�����Ӱ뾶��С��R3��<X��< M2��
B��Y��M��ɵĻ������ǹ⻯ѧ������ԭ��֮һ
C����YM2ͨ��Ba(NO3)2��Һ���д�����ɫ��������
D��M�⻯����۷е����Z�⻯����۷е�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡΫ���и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��6�֣�ˮ������֮Դ��Ҳ�ǻ�ѧ��Ӧ�����ǡ��Իش��������⣺
A��B��C����ѧ��ѧ������������ɫ���ʣ������Ԫ�ؾ����ڶ�����Ԫ�أ���Ħ�����������������Ǿ�����ˮ����������ԭ��Ӧ����ˮ�Ȳ���������Ҳ���ǻ�ԭ������д��A��B��C��ˮ��Ӧ�Ļ�ѧ����ʽ��
��1��A +H2O:__________________����2��B+H2O:_________________����3��C +H2O:___________ ___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com