
·ÖĪö £Ø1£©øł¾Żn=cV¼ĘĖć³öŃĪĖįÖŠŗ¬ÓŠHClµÄĪļÖŹµÄĮ棬øł¾Żn=$\frac{V}{{V}_{m}}$¼ĘĖć³öÉś³ÉĒāĘųµÄĪļÖŹµÄĮ棬¾Ż“ĖÅŠ¶ĻŃĪĖįŹĒ·ń¹żĮæ£¬Č»ŗó·Ö±šøł¾ŻŗĻ½š×ÜÖŹĮæ”¢Éś³ÉĒāĘųµÄĮæĮŠŹ½¼ĘĖć£»
£Ø2£©øł¾ŻĒāŌŖĖŲŹŲŗć¼ĘĖć³öĻūŗÄHClµÄĪļÖŹµÄĮ棬ŌŁøł¾ŻV=$\frac{n}{c}$¼ĘĖć³öĻūŗÄŃĪĖįµÄĢå»ż£»
£Ø3£©³Įµķ“ļµ½×ī“óŹ±ČÜŅŗÖŠČÜÖŹĪŖNaCl£¬øł¾Żn£ØNaOH£©=n£ØNaCl£©=n£ØHCl£©¼ĘĖć³öĻūŗÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮ棬ŌŁøł¾ŻV=$\frac{n}{c}$¼ĘĖć³öŠčŅŖ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗµÄĢå»ż£»
£Ø4£©ŌŁ¼ÓČėNaOHČÜŅŗÖĮ×ćĮ棬ĒāŃõ»ÆĀĮČܽā£¬×īŗóŹ£ÓąµÄ³ĮµķŹĒĒāŃõ»ÆĆ¾£¬øł¾ŻĆ¾ŌŖĖŲŹŲŗć¼ĘĖć³öĒāŃõ»ÆĆ¾µÄÖŹĮ森
½ā“š ½ā£ŗ£Ø1£©1L 5mol/LµÄŃĪĖįÖŠŗ¬ÓŠHClµÄĪļÖŹµÄĮæĪŖ£ŗ5mol/L”Į1L=5mol£¬±ź×¼×“æöĻĀ22.4LĒāĘųµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{22.4L}{22.4L/mol}$=1mol£¬Éś³É1molĒāĘųĻūŗÄ2molHCl£¬ĖµĆ÷ŃĪĖį¹żĮ棬ÉčŗĻ½šÖŠŗ¬ÓŠMg”¢AlµÄĪļÖŹµÄĮæ·Ö±šĪŖx”¢y£¬Ōņ£ŗ24x+27y=21”¢x+1.5y=1£¬ĮŖĮ¢½āµĆ£ŗx=0.5mol”¢y=$\frac{1}{3}$mol£¬
ŌņŗĻ½šÖŠŗ¬ÓŠĆ¾µÄÖŹĮæĪŖ£ŗ24g/mol”Į0.5mol=12g£¬ŗ¬ÓŠĀĮµÄÖŹĮæĪŖ£ŗ27g/mol”Į$\frac{1}{3}$mol=9g£¬
¹Ź“š°øĪŖ£ŗ12g£»9g£»
£Ø2£©Éś³É1molĒāĘųŠčŅŖĻūŗÄ2molHCl£¬Ōņ·“Ó¦ÖŠ¹²ĻūŗÄ5mol/LµÄŃĪĖįµÄĢå»żĪŖ£ŗ$\frac{2mol}{5mol/L}$=0.4L=400mL£¬
¹Ź“š°øĪŖ£ŗ400£»
£Ø3£©Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠÖšµĪ¼ÓČė5mol/LµÄNaOHČÜŅŗ£¬ČōŅŖŹ¹³ĮµķĒ”ŗĆ“ļµ½×ī“óÖµŹ±ČÜŅŗÖŠČÜÖŹĪŖNaCl£¬øł¾ŻÖŹĮæŹŲŗćæÉµĆ£ŗn£ØNaOH£©=n£ØNaCl£©=n£ØHCl£©=5mol£¬ŌņŠčŅŖ¼ÓČėNaOHµÄĢå»żĪŖ£ŗ$\frac{5mol}{5mol/L}$=1L£¬
¹Ź“š°øĪŖ£ŗ1£»
£Ø4£©ŌŁ¼ÓČėNaOHČÜŅŗÖĮ×ćĮ棬ĒāŃõ»ÆĀĮČܽā£¬Ōņ×īŗóŹ£ÓąµÄ³ĮµķŹĒĒāŃõ»ÆĆ¾£¬øł¾ŻÖŹĮæŹŲŗć¶ØĀÉæÉÖŖÉś³ÉĒāŃõ»ÆĆ¾µÄĪļÖŹµÄĮæĪŖ0.5mol£¬ÖŹĮæĪŖ£ŗ58g/mol”Į0.5mol=29g£¬
¹Ź“š°øĪŖ£ŗĒāŃõ»ÆĆ¾£»29£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ģŗĻĪļ·“Ó¦µÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č··¢Éś·“Ó¦µÄŌĄķĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕŹŲŗćĖ¼ĻėŌŚ»Æѧ¼ĘĖćÖŠµÄÓ¦ÓĆ·½·Ø£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®


 Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢ŁÖŠµÄI2ĪŖ¹ĢĢ¬£¬¢ŚÖŠµÄI2ĪŖĘųĢ¬ | |
| B£® | ¢ŚµÄ·“Ó¦Īļ×ÜÄÜĮæ±Č¢ŁµÄ·“Ó¦Īļ×ÜÄÜĮæµĶ | |
| C£® | ¢ŁµÄ²śĪļ±Č¢ŚµÄ²śĪļČČĪČ¶ØŠŌøüŗĆ | |
| D£® | 1 mol¹ĢĢ¬µāÉż»ŖŹ±½«ĪüČČ17 kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 6 gŃõĘųŗĶ³ōŃõ£ØO3£©µÄ»ģŗĻĘųĖłŗ¬µÄŌ×ÓŹżÄæĪŖNA | |
| B£® | ŗ¬ÓŠNAøöŗ¤Ō×ÓµÄŗ¤ĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ11.2L | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4 LĖ®ŗ¬ÓŠ1mol Ė®·Ö×Ó | |
| D£® | 22 gCO2Óė±ź×¼×“æöĻĀ11.2 L HClŗ¬ÓŠĻąĶ¬µÄŌ×ÓŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3ČÜŅŗ | B£® | äåĖ® | C£® | ŠĀÖĘCu£ØOH£©2 | D£® | ø£¶ūĀķĮÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.0”Į10-3mol/LŃĪĖįµÄpH=3.0£¬1.0”Į10-8mol/LŃĪĖįµÄpH=8.0 | |
| B£® | ŌŚ“×ĖįČÜŅŗµÄpH=a£¬½«“ĖČÜŅŗĻ”ŹĶ1±¶ŗó£¬ČÜŅŗµÄpH=b£¬Ōņa£¾b | |
| C£® | ŌŚµĪÓŠ·ÓĢŖČÜŅŗµÄ°±Ė®Ąļ£¬¼ÓČėNH4ClÖĮČÜŅŗĒ”ŗĆĪŽÉ«£¬Ōņ“ĖŹ±ČÜŅŗµÄpH£¼7 | |
| D£® | ³£ĪĀČō1mLpH=1µÄŃĪĖįÓė100mLNaOHČÜŅŗ»ģŗĻŗó£¬ČÜŅŗµÄpH=7ŌņNaOHČÜŅŗµÄpH=11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KClO3·Ö½āµĆŃõĘų | B£® | NaHSO4¼ÓČČČŪ»Æ | C£® | KHSO4¾§ĢåČÜÓŚĖ® | D£® | NH4ClŹÜČČ·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
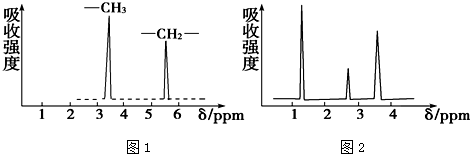
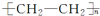
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com