
| A�� | �ֺ�Ա�Ȳ�ʱע���H2O��Ħ��������18�� | |
| B�� | H2O+Cl2?HCl+HClO�ⷴӦ����������ԭ��Ӧ | |
| C�� | �������ͬλ��1H��2D��3T��18Oֻ���γ�����ˮ���� | |
| D�� | �ڱ�״���£�1molˮ�����Լ��22.4L |
���� A��Ħ�������ĵ�λΪg/mol��
B���е���ת�ƵĻ�ѧ��Ӧ��������ԭ��Ӧ������������Ԫ�ػ��ϼ�������
C������ˮ���ӵĹ��ɽ��з�����һ��ˮ�����к���������ԭ�Ӻ�һ����ԭ�ӣ�ˮ���������е���ԭ�ӿ�����ͬһ����ԭ�ӣ�Ҳ�����Dz�ͬ����ԭ�ӣ�
D����״���£�ˮΪҺ�壮
��� �⣺A��Ħ�������ĵ�λΪg/mol������H2O��Ħ��������18g/mol����A����
B���÷�Ӧ��ClԪ�ػ��ϼ���0�۱�Ϊ-1�ۡ�+1�ۣ����������������������ǻ�ԭ����Ϊ������ԭ��Ӧ����B��ȷ��
C��һ��ˮ�����к���������ԭ�Ӻ�һ����ԭ�ӣ�ˮ���������е���ԭ�ӿ�����ͬһ����ԭ�ӣ�Ҳ�����Dz�ͬ����ԭ�ӣ�����ͬһ����ԭ�ӣ�������ɵ�ˮ����������3�֣����Dz�ͬ����ԭ�ӣ�����1H��2D��ɵ�ˮ������1�֣���2D��3H��ɵ�ˮ������1�֣���1H��3H��ɵ�ˮ������1�֣�����6��ˮ���ӣ���C����
D����״���£�ˮΪҺ�壬1molˮ�����Լ��18mL����D����
��ѡB��
���� ���⿼���Ϊ�ۺϣ��漰Ħ��������������ԭ��Ӧ��ͬλ���Լ����ʵ����ļ����֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬�ѶȲ���ע�����֪ʶ��ѧϰ�ͻ��ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
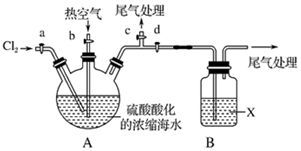
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
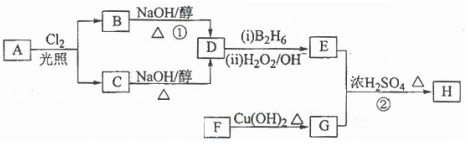
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ���KI��ֽ������������NO2���� | |
| B�� | ֤��Fe2O3�Ǽ���������ɽ����������ϣ��۲����� | |
| C�� | ��NaOH��Һ����մ��Ƥ���ϣ�Ӧ�������ô�����������ϴ | |
| D�� | ��ȥMnO2�е�����KMnO4���ɽ���������ˮ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���Ϸ������Ƿ��ȷ�Ӧ | B�� | ���콫��ѧ��ת��Ϊ̫���� | ||
| C�� | ���Ͻ���ѧ��ת��Ϊ���� | D�� | �˷��ɼ�������������ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
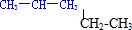 ��뭡�뮺��
��뭡�뮺���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ����ǰһ��Ҫ���������Ĵ��� | |
| B�� | δʹ����İ���Ҫ��ʱ�ռ������������������ | |
| C�� | �ƾ��Ʋ���ʱ��������ϵ�ñ | |
| D�� | ��CO��ԭ������ʱ��Ҫ��ͨһ���CO���壬�ټ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ��ʱ��ϵ�����ı仯 | ||
| N2 | H2 | NH3 | ||
| ��1�� | 2 | 3 | 0 | 27.78kJ |
| ��2�� | 1.6 | 1.8 | 0.8 | Q |
| A�� | ������2���з�Ӧ��ʼʱv��������v���棩 | |
| B�� | ������1������2���з�Ӧ��ƽ��ʱѹǿ��� | |
| C�� | ������2���з�Ӧ��ƽ��ʱ�����յ�����QΪ9.26 kJ | |
| D�� | ������Ϊ�����Ⱥ��ݡ���������1���з�Ӧ��ƽ��ʱn ��NH3����0.6 mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com