
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )
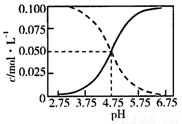
A.25℃时,CH3COOH的电离常数K的值5×10-2.75
B.随pH增大, 增大
增大
C.pH=4的溶液中,c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.pH=5的溶液中,c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol•L-1
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2015-2016学年广东汕头金山中学高二下第十二周练化学卷(解析版) 题型:填空题
第四周期的许多金属能形成配合物。科学家通过X射线测得胆矾结构示意图可简单表示如下: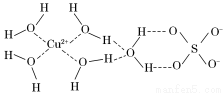
(1)Cu基态原子的外围电子排布为 ,Cr基态原子的外围电子排布为 ,这样排布的理由是_____________________。
(2)NH3是一种很好的配体,原因是______________________。
(3)图中虚线表示的作用力为________________。
(4)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在该晶体中,含有的原子团或分子有:[Cu(NH3)4]2+、NH3、SO42-、H2O,其中[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团或分子是__________,写出一种与此正四面体结构互为等电子体的分子的分子式 。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于________(填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:计算题
有机物A由碳、氢、氧三种元素组成。现取3克A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6克, 碱石灰增重4.4克。回答下列问题:(要有计算过程)
(1)3克A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中理科化学试卷(解析版) 题型:选择题
下列说法正确的是
A.实验室制取乙烯时浓硫酸是催化剂和吸水剂
B.硝基苯制备时浓硫酸作催化剂和脱水剂
C.实验室制备乙烯、硝基苯、苯磺酸时均使用到温度计,且水银球在反应混合物液面以下
D.水浴加热的优点是可以受热均匀且便于控制温度
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:填空题
有机化合物K在化工和医药方面有重要的应用,其合成路线如下:

已知信息:
①C能发生银镜反应,E的相对分子质量比D大4,G的苯环上的一溴代物有两种
②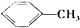
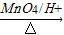

③2RCH2CHO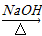
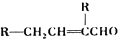
请回答下列问题:
(1)F的名称是__________,H含有的官能团是__________。
(2)A→B的反应类型是__________,F→G的反应类型是__________。
(3)C与银氨溶液反应的化学方程式是__________。
(4)K的结构简式是__________。
(5)符合下列要求的C8H10O的同分异构体有__________种.
①芳香族化合物②与Na反应并产生H2③遇FeCl3溶液呈紫色,
其中核磁共振氢谱为4组峰,且面积比为6:2:1:1的是__________(写出其中一种结构简式)
(6)参照已知信息和成路线,设计一条由CH2=CH2为原料合成CH3CH2CH2CH2OH的路线(注明反应条件):__________。
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值.下列说法正确的是( )
A.1 mol-OH(羟基)与l mol NH4+中所含电子数均为10NA
B.25℃时,100 mL pH=l的稀硫酸中,含有的H+数目为0.01 NA
C.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1 NA
D.标准状况下,2.24LNO2和N2O4混合气体中含0.2 NA个氧原子
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练三化学试卷(解析版) 题型:选择题
某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g) 3Z(g)。平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g)。平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A.m=2
B.第二次平衡时,Z的浓度为0.4 mol·L-1
C.两次平衡的平衡常数相同
D.X与Y的平衡转化率之比为1∶1
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列事实不能用元素周期律解释的是
A.向Na2SO3溶液中加盐酸,有气泡产生
B.0.1 mol•L-1溶液的pH:NaOH>LiOH
C.Mg、Al与同浓度盐酸反应,Mg更剧烈
D.气态氢化物的稳定性:HBr>HI
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:填空题
Ⅰ、单质硅由于其成熟的生产工艺, 丰富的生产原料及优异的性能被广泛用于电子行业及太阳能电池的生产等,在二氧化碳氛围中通过利用金属钠来还原二氧化硅可在较低的温度条件下得到硅,同时生成一种盐X,这相比起现有的生产工艺具有节约能耗的优势。
(1)写出上述制备硅的化学反应方程式 。
(2)二氧化硅与二氧化碳物理性质差别很大,原因是 。
(3)盐X的溶液能与Al2(SO4)3溶液反应生成一种白色沉淀和气体。写出此反应的离子反应方程式 。
Ⅱ、某盐A有3种元素组成,易溶于水。将A加热,生成既不助燃,也不使湿润的红色或蓝色石蕊试纸变色的气体B和H2O。将A溶于水,进行下列实验:①酸性条件下与H2S作用生成淡黄色沉淀C,同时放出无色气体D,D在空气中转变为红棕色气体E;②当通入足量Cl2时,无明显现象,但将所得溶液浓缩后即可得到无色晶体盐F。请回答下列问题:
(1)写出A的化学式: ; B的电子式: 。
(2)写出上述实验①、②所发生的离子反应方程式:
① ;② 。
(3)D、E对环境有危害,可用NaOH溶液来吸收等物质的量的D、E混合气体,写出其化学反应方程式 。
(4)判断盐F的可能成份 ;设计实验方案确定F的成份 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com