
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: 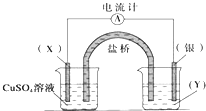
(1)电极X的材料是 , 电解质溶液Y是;
(2)银电极为电池的极,发生的电极反应为X电极上发生的电极反应为 .
(3)外电路中的电子是从电极流向电极.
【答案】
(1)Cu;AgNO3
(2)正;2Ag++2e﹣═2Ag;Cu﹣2e﹣═Cu2+
(3)Cu;Ag
【解析】解:(1)由反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)可知,在反应中,Cu被氧化,失电子,应为原电池的负极,所以X电极材料是Cu,Ag+在正极上得电子被还原,电解质溶液为AgNO3 , 所以答案是:Cu;AgNO3;(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为2Ag++2e﹣═2Ag,X(铜)电极失电子发生氧化反应,电极反应为Cu﹣2e﹣═Cu2+ ,
所以答案是:正极; 2Ag++2e﹣=2Ag;Cu﹣2e﹣═Cu2+;(3)电子从负极Cu沿导线流向正极Ag,
所以答案是:Cu;Ag.


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 2.4 g金属镁与足量盐酸反应,转移电子的数目为0.1 NA
B. 1L 1 mol·L-1的CaCl2溶液中含Cl-的数目为NA
C. 在25℃、1.01×105Pa的条件下,2.24 L H2中含有的分子数小于0.1 NA
D. 22 g CO2与标准状况下11.2 L H2O含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含少量Na2CrO4,考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置,使浆液分离成固体混合物和含铬元素溶液,并回收利用。已知:阴极池中得到NaOH和H2,阳极池中得到含有Cr2O72-和CrO42-的混合溶液。

(1)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是____________________。
(2)离子交换膜I属于________________(填“阳膜”或“阴膜”),阳极的电极反应方程式为___。生成Cr2O72-的原因____________(离子反应方程式和必要的文字解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡.
请根据所学知识的回答:
(1)浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4③HCOOH ④Ba(OH)2⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl 溶液pH值由小到大的顺序是(填写编号) .
(2)B为0.1molL﹣1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请用离子方程式表示其原因: .
(3)在0.10molL﹣1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=(已知Ksp[Cu(OH)2]=2.2x10﹣20).若在0.10molL﹣1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cl2制成漂白粉的最主要目的是:①使它转变成较易溶于水的物质 ②转变成较稳定、便于贮存的物质 ③提高氯的质量分数 ④提高漂白能力
A.①②③B.②④C.②③D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2气体通入下列澄清溶液中,最终仍为澄清溶液的是( )
A. 偏铝酸钠溶液 B. 氯化钡溶液 C. 含有氨水的NaCl饱和溶液 D. 饱和Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com