
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦![]()
![]()
![]()
![]() ”£Ņ»¶ØĢõ¼žĻĀ£¬ĻņČŻ»żĪŖ
”£Ņ»¶ØĢõ¼žĻĀ£¬ĻņČŻ»żĪŖ![]() µÄĆܱÕČŻĘ÷ÖŠ³äČė
µÄĆܱÕČŻĘ÷ÖŠ³äČė![]() ŗĶ
ŗĶ![]() £¬²āµĆ
£¬²āµĆ![]() ŗĶ
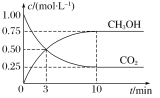
ŗĶ![]() µÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
µÄÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
A.ÉżøßĪĀ¶ČÄÜŹ¹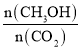 Ōö“ó
Ōö“ó
B.·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬![]() µÄ×Ŗ»ÆĀŹĪŖ75%
µÄ×Ŗ»ÆĀŹĪŖ75%
C.![]() Ź±£¬ÓĆ
Ź±£¬ÓĆ![]() ±ķŹ¾µÄÕż·“Ó¦µÄ·“Ó¦ĖŁĀŹµČÓŚÓĆ
±ķŹ¾µÄÕż·“Ó¦µÄ·“Ó¦ĖŁĀŹµČÓŚÓĆ![]() ±ķŹ¾µÄÄę·“Ó¦µÄ·“Ó¦ĖŁĀŹ
±ķŹ¾µÄÄę·“Ó¦µÄ·“Ó¦ĖŁĀŹ
D.“Ó·“Ó¦æŖŹ¼µ½·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬![]() µÄĘ½¾ł·“Ó¦ĖŁĀŹ
µÄĘ½¾ł·“Ó¦ĖŁĀŹ![]()
”¾“š°ø”æB
”¾½āĪö”æ
A”¢øĆ·“Ó¦![]() £¬ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬
£¬ĪŖ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬![]() ¼õŠ”£¬
¼õŠ”£¬![]() Ōö“ó£¬
Ōö“ó£¬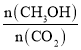 ¼õŠ”£¬AĻī“ķĪó£»
¼õŠ”£¬AĻī“ķĪó£»
B”¢·“Ó¦“ļµ½»ÆŃ§Ę½ŗāŹ±£¬![]() µÄ×Ŗ»ÆĀŹĪŖ
µÄ×Ŗ»ÆĀŹĪŖ![]() £¬BĻīÕżČ·£»
£¬BĻīÕżČ·£»
C”¢![]() Ź±£¬
Ź±£¬![]() £¬ÓÉÓŚ
£¬ÓÉÓŚ![]() ŗó
ŗó![]() Ōö“ó£¬
Ōö“ó£¬![]() ¼õŠ”£¬¼“
¼õŠ”£¬¼“![]() £¬Ņņ“ĖÓĆ
£¬Ņņ“ĖÓĆ![]() ±ķŹ¾µÄÕż·“Ó¦µÄ·“Ó¦ĖŁĀŹ“óÓŚÓĆ
±ķŹ¾µÄÕż·“Ó¦µÄ·“Ó¦ĖŁĀŹ“óÓŚÓĆ![]() ±ķŹ¾µÄÄę·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬CĻī“ķĪó£»
±ķŹ¾µÄÄę·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬CĻī“ķĪó£»
D”¢![]() ÄŚ£¬
ÄŚ£¬![]() £¬øł¾ŻĶ¬Ņ»·“Ó¦ÖŠ²»Ķ¬ĪļÖŹµÄ·“Ó¦ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬
£¬øł¾ŻĶ¬Ņ»·“Ó¦ÖŠ²»Ķ¬ĪļÖŹµÄ·“Ó¦ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬![]() £¬DĻī“ķĪó£»
£¬DĻī“ķĪó£»
¹ŹŃ”B”£


 ÖĒ»ŪŠ”ø“Ļ°ĻµĮŠ“š°ø
ÖĒ»ŪŠ”ø“Ļ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦µÄŠšŹöĻą·ūµÄŹĒ
A.Ķ¼±ķŹ¾·“Ó¦2SO2 (g)£«O2(g)![]() 2SO3 (g) ¦¤H£¼0²»Ķ¬ĪĀ¶Č£ØT1£¼T2£©Ź±Ę½ŗā³£ŹżKĖęŃ¹ĒæµÄ±ä»Æ¹ŲĻµĶ¼
2SO3 (g) ¦¤H£¼0²»Ķ¬ĪĀ¶Č£ØT1£¼T2£©Ź±Ę½ŗā³£ŹżKĖęŃ¹ĒæµÄ±ä»Æ¹ŲĻµĶ¼
B.Ķ¼ĒśĻß±ķŹ¾µē½ā¾«Į¶Ķ¹ż³ĢÖŠµē¼«ÖŹĮæµÄ±ä»Æ
C.Ķ¼ĒśĻß±ķŹ¾·“Ó¦N2(g)£«3H2(g)![]() 2NH3(g)ŌŚt1Ź±æĢŌö“óŃ¹Ēæŗóv(Õż)”¢v(Äę)Ėꏱ¼äµÄ±ä»Æ
2NH3(g)ŌŚt1Ź±æĢŌö“óŃ¹Ēæŗóv(Õż)”¢v(Äę)Ėꏱ¼äµÄ±ä»Æ
D.Ķ¼ĒśĻß±ķŹ¾0.1000 mol”¤L”Ŗ1 NaOHČÜŅŗµĪ¶Ø20.00 mL pH£½£±µÄCH3COOHČÜŅŗĖłµĆČÜŅŗµÄpHĖęNaOHČÜŅŗĢå»żµÄ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCu(OH)2ŌŚĖ®ČÜŅŗÖŠ“ęŌŚ×ÅČēĻĀ³ĮµķČܽāĘ½ŗā£ŗCu(OH)2(s) Cu2£«(aq)£«2OH£(aq)£¬ŌŚ³£ĪĀĻĀKsp£½2”Į10£20”£ŌŚ³£ĪĀĻĀČē¹ūŅŖÉś³ÉCu(OH)2³Įµķ£¬ŠčŅŖĻņ0.02mol/LµÄCuSO4ČÜŅŗÖŠ¼ÓČė¼īĄ“µ÷ÕūČÜŅŗµÄpH£¬Ó¦Ź¹ČÜŅŗµÄpH“óÓŚ( )
A.3B.4C.5D.6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»øöĢå»żĪŖ5 LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ¼ÓČė1.25 mol CaCO3£¬·¢Éś·“Ó¦CaCO3 (s)![]() CaO(s) +CO2(g)£¬²āµĆĘ½ŗāŹ±¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæÅضČĖęĪĀ¶ČµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
CaO(s) +CO2(g)£¬²āµĆĘ½ŗāŹ±¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæÅضČĖęĪĀ¶ČµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
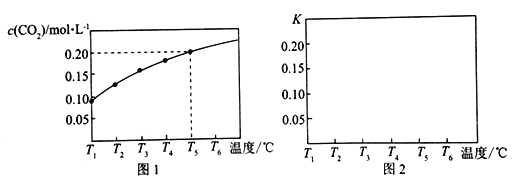
Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦Õż·“Ó¦ĪŖ__________ČČ·“Ó¦£ØĢī”°Īü”±»ņ”°·Å”±£©£¬ĪĀ¶ČĪŖT5”ꏱ£¬øĆ·“Ó¦ŗÄŹ±40s“ļµ½Ę½ŗā£¬ŌņT5”ꏱ£¬øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ________________”£
£Ø2£©T2”ꏱ£¬øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗā£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹øĆ·“Ó¦µÄĘ½ŗā³£ŹżKÖµ±ä“óµÄŹĒ_______________(Ń”Ģī±ąŗÅ)”£
a.¼õŠ”Ń¹Ēæ b.¼õÉŁCaOµÄĮæ c.¼ÓČėCaCO3 d.ÉżøßĪĀ¶Č
£Ø3£©ĒėŌŚČēĶ¼ÖŠ»³öĘ½ŗā³£ŹżKĖęĪĀ¶ČµÄ±ä»ÆĒśĻß_______________”£
£Ø4£©ŌŚT5”ęĻĀ£¬Ī¬³ÖĪĀ¶ČŗĶČŻĘ÷Ģå»ż²»±ä£¬ĻņÉĻŹöĘ½ŗāĢåĻµÖŠŌŁ³äČė1molN2£¬Ōņ×īŗóĘ½ŗāŹ±ČŻĘ÷ÖŠµÄCaCO3µÄÖŹĮæĪŖ________g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌÄų·ĻĮĻ(Ö÷ŅŖ³É·ÖĪŖÄųĢśŗĻ½š£¬ŗ¬ÉŁĮæĶ)ĪŖŌĮĻ£¬Éś²śNiOµÄ²æ·Ö¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
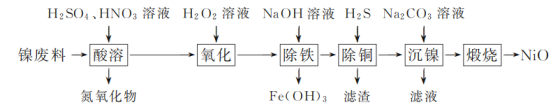
ŅŃÖŖ£ŗĻĀ±ķĮŠ³öĮĖ¼øÖÖ½šŹōĄė×ÓÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH(æŖŹ¼³ĮµķµÄpH°“½šŹōĄė×ÓÅضČĪŖ1.0 mol”¤L£1¼ĘĖć)”£
ĒāŃõ»ÆĪļ | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
æŖŹ¼³ĮµķµÄpH | 1.5 | 6.5 | 7.7 |
³ĮµķĶźČ«µÄpH | 3.3 | 9.9 | 9.2 |
£Ø1£©”°³żĢś”±Ź±ŠčæŲÖĘČÜŅŗµÄpH·¶Ī§ĪŖ________”£
£Ø2£©”°ĀĖŌü”±µÄÖ÷ŅŖ³É·ÖĪŖ________(Ģī»ÆѧŹ½)”£
£Ø3£©”°³ĮÄų”±Ź±µĆµ½¼īŹ½Ģ¼ĖįÄų[ÓĆxNiCO3”¤yNi(OH)2±ķŹ¾]³Įµķ”£
¢ŁŌŚøō¾ųæÕĘųĢõ¼žĻĀ£¬”°ģŃÉÕ”±¼īŹ½Ģ¼ĖįÄųµĆµ½NiO£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________”£
¢Ś”°³ĮÄų”±Ź±£¬ČÜŅŗpHŌö“󣬼īŹ½Ģ¼ĖįÄųÖŠNiŌŖĖŲŗ¬Įæ»įŌö¼Ó£¬ŌŅņŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ2H2(g)£«O2(g)===2H2O(l) ¦¤H£½£571.6kJ”¤mol£1
CO(g)£«1/2O2(g)===CO2(g) ¦¤H£½£282.8kJ”¤mol£1
ĻÖÓŠCO”¢H2”¢CO2×é³ÉµÄ»ģŗĻĘųĢå67.2L(±ź×¼×“æö)£¬¾ĶźČ«Č¼ÉÕŗó·Å³öµÄ×ÜČČĮæĪŖ710.0kJ£¬²¢Éś³É18gŅŗĢ¬Ė®£¬ŌņČ¼ÉÕĒ°»ģŗĻĘųĢåÖŠCOµÄĢå»ż·ÖŹżĪŖ(””””)
A. 80% B. 50% C. 60% D. 20%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCO2µÄ׏Ō“»ÆĄūÓĆÄÜÓŠŠ§¼õÉŁCO2ÅÅ·Å£¬³ä·ÖĄūÓĆĢ¼×ŹŌ“”£
£Ø3£©CO2“߻ƼÓĒāŗĻ³É¶ž¼×ĆŃŹĒŅ»ÖÖCO2×Ŗ»Æ·½·Ø£¬Ęä¹ż³ĢÖŠÖ÷ŅŖ·¢ÉśĻĀĮŠ·“Ó¦£ŗ
·“Ó¦¢ń£ŗCO2(g)+H2(g)![]() CO(g)+H2O(g) ¦¤H =41.2 kJ”¤mol1
CO(g)+H2O(g) ¦¤H =41.2 kJ”¤mol1
·“Ó¦¢ņ£ŗ2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ¦¤H =©122.5 kJ”¤mol1
CH3OCH3(g)+3H2O(g) ¦¤H =©122.5 kJ”¤mol1
ŌŚŗćŃ¹”¢CO2ŗĶH2µÄĘšŹ¼ĮæŅ»¶ØµÄĢõ¼žĻĀ£¬CO2Ę½ŗā×Ŗ»ÆĀŹŗĶĘ½ŗāŹ±CH3OCH3µÄŃ”ŌńŠŌĖęĪĀ¶ČµÄ±ä»ÆČēĶ¼”£ĘäÖŠ£ŗCH3OCH3µÄŃ”ŌńŠŌ=![]() ”Į100£„
”Į100£„
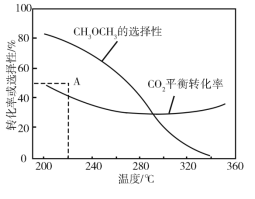
¢ŁĪĀ¶ČøßÓŚ300 ”ę£¬CO2Ę½ŗā×Ŗ»ÆĀŹĖęĪĀ¶ČÉżø߶ųÉĻÉżµÄŌŅņŹĒ________”£
¢Ś220 ”ꏱ£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀCO2ÓėH2·“Ó¦Ņ»¶ĪŹ±¼äŗ󣬲āµĆCH3OCH3µÄŃ”ŌńŠŌĪŖ48%£ØĶ¼ÖŠAµć£©”£²»øı䷓ӦŹ±¼äŗĶĪĀ¶Č£¬Ņ»¶ØÄÜĢįøßCH3OCH3Ń”ŌńŠŌµÄ“ėŹ©ÓŠ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲÄÜĮæµÄŠšŹö²»ÕżČ·µÄŹĒ
A.H2(g)µÄČ¼ÉÕČČŹĒH=-285.8kJ/mol£¬Ōņ·“Ó¦2H2O(g)=2H2(g)+O2(g)µÄ·“Ó¦ČČH=+571.6kJ/mol
B.»Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³ÉŹĒĪļÖŹŌŚ»Æѧ±ä»ÆÖŠÄÜĮæ±ä»ÆµÄÖ÷ŅŖŌŅņ
C.»ī»ÆÄܵē󊔶Ō»Æѧ·“Ó¦Ē°ŗóµÄÄÜĮæ±ä»Æ²»²śÉśÓ°Ļģ
D.»Æѧ·“Ó¦¹ż³ĢÖŠĶ¬Ź±“ęŌŚĪļÖŹ±ä»ÆŗĶÄÜĮæµÄ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĪŖ¼øÖÖ¾§Ģå»ņ¾§°ūµÄŹ¾ŅāĶ¼£ŗ


Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÉĻŹö¾§ĢåÖŠ£¬Į£×ÓÖ®¼äŅŌ¹²¼Ū¼ü½įŗĻŠĪ³ÉµÄ¾§ĢåŹĒ____”£
£Ø2£©±ł”¢½šøÕŹÆ”¢MgO”¢CaCl2”¢øɱł5ÖÖ¾§ĢåµÄČŪµćÓÉøßµ½µĶµÄĖ³ŠņĪŖ£ŗ___”£
£Ø3£©NaCl¾§°ūÓėMgO¾§°ūĻąĶ¬£¬NaCl¾§ĢåµÄ¾§øńÄÜ___(Ģī”°“óÓŚ”±»ņ”°Š”ÓŚ”±)MgO¾§Ģ壬ŌŅņŹĒ____”£
£Ø4£©ĆæøöCu¾§°ūÖŠŹµ¼ŹÕ¼ÓŠ___øöCuŌ×Ó£¬CaCl2¾§ĢåÖŠCa2£«µÄÅäĪ»ŹżĪŖ__”£
£Ø5£©±łµÄČŪµćŌ¶øßÓŚøɱł£¬³żH2OŹĒ¼«ŠŌ·Ö×Ó”¢CO2ŹĒ·Ē¼«ŠŌ·Ö×ÓĶā£¬»¹ÓŠŅ»øöÖŲŅŖµÄŌŅņŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com