
 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | 离O点越远的元素原子半径越大 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | B元素是图中金属性最强的元素 | |
| D. | A、B组成的化合物中阴阳离子的个数比都是1:2 |
分析 0点代表氢元素,按照原子序数由小到大由里往外延伸,由图可知,A为第8号元素,为O元素;B为11号元素,为O元素;O、B连线的三元素为第ⅠA族,根据元素的种类可知虚线相连的元素处于同一族,结合对应元素的性质解答该题.
解答 解:0点代表氢元素,按照原子序数由小到大由里往外延伸,由图可知,A为第8号元素,为O元素;B为11号元素,为O元素;O、B连线的三元素为第ⅠA族,根据元素的种类可知虚线相连的元素处于同一族,
A.离O点越远的元素原子的核电荷数增大,若电子层相同,半径越小,故A错误;
B.由原子序数可知,虚线相连的元素处于同一族,故B正确;
C.B为Na元素,是图中金属性最强的元素,故C正确;
D.钠与氧元素可以氧化钠、过氧化钠,氧化钠中阴阳离子个数之比为1:2,过氧化钠中阴阳离子个数之比为1:1,故D错误;
故选AD.
点评 本题考查元素周期表、元素周期律的综合应用,题目难度中等,看懂图象推断元素是解题的关键,注意对元素周期表的整体把握,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
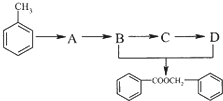
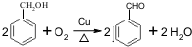 .
. 的化学方程式为
的化学方程式为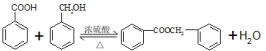 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Fe的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入水蒸气 | |
| D. | 压强不变,充入Ne使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂或试验方法 | 说明 |
| A | 从苯中提溴 | 加CCl4 | 溴易溶于CCl4 |
| B | 检验含Fe3+溶液中是否含Fe2+ | 加高锰酸钾溶液 | 溶液紫色褪去,说明含Fe2+ |
| C | 配置1mol/LFeCl3溶液100mL | 将一定质量FeCl3溶液转移至容量瓶中加水定容 | 容量瓶规格须为100mL |
| D | 制取漂白粉 | 将氯气通入澄清石灰水中 | 氯气与氢氧化钙反应生成次氯酸钙 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①③ | C. | 只有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
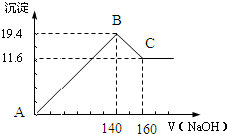
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Kw(NH3•H2O) | B. | n(OH-) | C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | D. | c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管和锥形瓶在使用前要用润洗 | |
| B. | 检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 | |
| D. | 将CO2和SO2混合气体分别通入BaC12溶液、Ba(NO3)2溶液中,最终都有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com