
【题目】如图所示装置,烧杯中盛有200mL1 mol/L的CuSO4溶液。

(1)正极材料为______,电池工作时SO42-向______移动(填Zn或Cu)。
(2)正极电极反应式为_______。
(3)若初始时Zn片与Cu片质量相等,实验结束后,称得两极质量差为12.9g,则反应中转移电子的物质的量为____,反应后溶液中溶质的物质的量浓度为________(忽略溶液体积的变化)。
【答案】Cu Zn Cu2++2e-=Cu 0.2mol c(ZnSO4)=0.5 mol/L,c(CuSO4)=0.5 mol/L
【解析】
(1)该装置是原电池,Zn易失电子作负极、Cu作正极,负极反应式为Zn-2e-=Zn2+、正极反应式为Cu2++2e-=Cu结合同种电荷相互排斥,异种电荷相互吸引的原则判断阴离子移动方向;
(2)在正极上溶液中的Cu2+获得电子,发生还原反应;
(3)负极上锌逐渐溶解、正极上析出Cu,所以两极质量差等于溶解锌的质量和析出铜的质量之和,再结合转移电子相等进行计算;根据原子守恒计算硫酸锌、硫酸铜浓度。
(1)该装置是原电池,由于金属活动性Zn>Cu,所以Zn易失电子作负极、Cu作正极。负极上锌失电子发生氧化反应生成锌离子,所以负极反应式为Zn-2e-=Zn2+、SO42-带负电荷,会向正电荷较多的负极区Zn电极方向移动;
(2)正极Cu上溶液中铜离子得电子发生还原反应生成Cu,所以正极反应式为Cu2++2e-=Cu;
(3)负极上锌逐渐溶解、正极上析出Cu,所以两极质量差等于溶解锌的质量和析出铜的质量之和,设溶解锌的物质的量为xmol,根据转移电子守恒可知:正极上析出Cu的物质的量也是xmol,则两个电极的质量差(65+64)g/mol×xmol=12.9g,解得x=0.1mol,所以转移电子的物质的量=0.1mol×2=0.2mol;溶解锌的物质的量为0.1mol、析出Cu的物质的量为0.1mol,则溶液中还剩余硫酸铜的物质的量为0.2L×1mol/L-0.1mol=0.1mol,根据原子守恒知,溶液中c(ZnSO4)=![]() =0.5 mol/L,c(CuSO4)=
=0.5 mol/L,c(CuSO4)=![]() 0.5 mol/L。
0.5 mol/L。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L1 HA中逐滴加入0.1 mol·L1 NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是
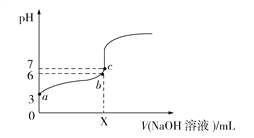
A. b点溶液中H2O电离出的H+浓度大于c点
B. Ka(HA)=106
C. b点溶液中有c(A)c(Na+)=9.9×107 mol·L1
D. c点溶液中的微粒只有A、OH、H+、Na+和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A. 标准状况下,14 g氮气含有的核外电子数为7 NA
B. 标准状况下,2.24 L![]() 与
与![]() 的混合物中含有的分子数为0.1 NA
的混合物中含有的分子数为0.1 NA
C. 常温常压下,7.8 g苯中含有双键的数目为0.3 NA
D. 常温下,1 L 0.1 ![]() 的
的![]() 溶液中氧原子数为0.3 NA
溶液中氧原子数为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,试按下述所给的条件推断:①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;②D、E是周期表中位置相邻的非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;③F是除氢外原子半径最小的主族元素。
(1)A元素的名称___,B元素在周期表中的位置为___,C元素的离子结构示意图_____。
(2)E元素的单质颜色_____。
(3)在上述六种元素最高价氧化物对应的水化物中,碱性最强的化学式______,酸性最强的化学式____,气态氢化物最稳定的化学式______。
(4)A、C元素最高价氧化物对应的水化物反应的离子方程式_______。
(5)用电子式表示A元素与D元素形成化合物的过程___________。
(6)F元素的单质与水反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到500 mL,关于稀释后的溶液叙述不正确的是( )
A. 浓度为0.03 mol·L-1 B. 从中取出10 mL溶液,其浓度为0.03 mol·L-1
C. 含NaOH 0.6 g D. 从中取出10 mL溶液,含NaOH 0.015 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学家们合成了一种新物质——五星烷,其键线式如图所示。下列有关五星烷的说法正确的是( )

A. 五星烷与乙烷互为同系物 B. 五星烷的化学式为C15H20
C. 五星烷的分子中含有7个五元环 D. 五星烷的一氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是( )
A.Al在空气中表面生成致密的氧化膜B.MnO2和稀盐酸反应制取Cl2
C.氢氟酸能用玻璃瓶存放D.室温下Na与空气中O2制取Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,请回答下列问题:
族/周期 | IA | IIA | III A | IVA | VA | VIA | VIIA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质最不活泼的是___________________(填元素符号),其⑤的离子结构示意图为____________________。
(2)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为____________(填物质的化学式),酸性最强的化合物为________________(填物质的化学式)。
(3)在②和③两种元素中,非金属性较强的是______(填元素名称),②的某种单质可以和③的最高价氧化物的水化物反应,请写出有关化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,下列叙述中正确的是

(1)a、b分别代表的意思是_______________、___________________。
(2)该反应ΔH_______________________
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为________________,干燥管D的作用为___________________。
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为________,观察到C中溶液____________ (填现象),即可证明。从环境保护的观点考虑,此装置缺点 __________。
(5)若要证明非金属性:S>C>Si,则在A中__________B中加_________、C中加__________,写出C中反应的化学方程式______________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com