
【题目】在元素周期表中金属与非金属的分界处,可以找到( )
A.合金B.农药C.催化剂D.半导体材料
科目:高中化学 来源: 题型:
【题目】在0.1L密闭容器中有0.1molSO2和0.05molO2发生反应,恒温下30min后达到平衡。
(1)若得到0.06molSO3,求达到平衡时SO2的浓度_______。
(2)求30min内的反应速率:v(SO3)、v(O2)_______。
(3)求平衡时气体压强与开始时气体压强之比_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫元素的几种化合物存在下列转化关系:
![]()
下列判断不正确的是
A. 反应①中浓硫酸作氧化剂 B. 反应②表明SO2有酸性氧化物的性质
C. 反应③的原子利用率是100% D. 反应④稀H2SO4作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源,CH4—H2O催化重整是目前大规模制取氢气的重要方法。
(1)CH4-H2O催化重整:
反应Ⅰ:CH4(g)+H2O(g)![]() CO(g)+3H2(g) H1 = +210kJ/mol
CO(g)+3H2(g) H1 = +210kJ/mol
反应Ⅱ: CO(g)+ H2O(g)![]() CO2(g)+H2(g) H2 =﹣41kJ/mol
CO2(g)+H2(g) H2 =﹣41kJ/mol
①提高CH4平衡转化率的条件是________。
a.增大压强 b.加入催化剂 c.增大水蒸气浓度
②CH4、H2O催化重整生成CO2、H2的热化学方程式是________。
③在密闭容器中,将2.0 mol CO与8.0 mol H2O混合加热到800℃发生反应Ⅱ,达到平衡时CO的转化率是80%,其平衡常数为 _________。
(2)实验发现,其他条件不变,相同时间内,向催化重整体系中投入一定量的CaO可以明显提高H2的百分含量。做对比实验,结果如下图所示:

①投入CaO时,H2百分含量增大的原因是:_________。
②投入纳米CaO时,H2百分含量增大的原因是:__________。
(3)反应中催化剂活性会因积炭反应而降低,相关数据如下表:
反应 | Ⅰ | Ⅱ |
|
| |
H(kJ/mol) | +75 | ﹣173 |
①研究发现,如果反应Ⅰ不发生积炭过程,则反应Ⅱ也不会发生积炭过程。因此,若保持催化剂的活性,应采取的条件是_________。
②如果Ⅰ、Ⅱ均发生了积炭反应,通入过量水蒸气能有效清除积炭,反应的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.浓硫酸在空气中敞口放置一段时间,浓度变小
B.铁片投入冷的浓硝酸中,铁片不溶解
C.铜片投入浓硝酸中,产生红棕色气体
D.石蕊溶液滴入稀硫酸中,溶液变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过所学知识,回答下面问题
(1)写出铁与水蒸气在高温下反应方程式_______________________________________。
(2)加热碳酸氢钠的化学方程式为______________________________________
(3)在呼吸面具中,Na2O2起反应的化学方程式为__________________。当有7.8克Na2O2反应时,放出氧气的质量为__________。
(4)将铜片投入到FeCl3溶液中恰好完全反应,发生的反应离子方程式为___________。
(5)向FeSO4溶液中滴加NaOH溶液时,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色。写出此变化过程的化学方程式: __________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)已知2A2(g)+B2(g)![]() 2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡时放出热量b kJ。
2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡时放出热量b kJ。
(1)比较a___b(填“>、=、<”)
(2)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
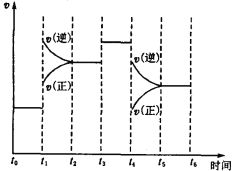
(3)下图表示此反应的反应速率v和时间t的关系图。根据下图判断,在t1和t4时刻改变的外界条件分别是_______________和 _____________ 。
(二)在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)![]() 2NH3(g);△H<0。反应中NH3的物质的量浓度的变化情况如右图所示,请回答下列问题:
2NH3(g);△H<0。反应中NH3的物质的量浓度的变化情况如右图所示,请回答下列问题:
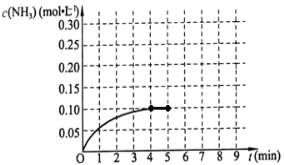
(1)根据上图,该反应达到平衡时H2的转化率等于__________。
(2)第5分钟末,保持其它条件不变,若改变反应温度,达新平衡后NH3的物质的量浓度不可能为_________。(填序号)。
a 0.20mol·L-1 b 0.12 mol·L-1 c 0.10 mol·L-1 d 0.08 mol·L-1
(3)若在第5分钟末将容器的体积缩小一半后,在第8分钟达到新的平衡(此时NH3的浓度约为0.25 mol·L-1 ),请在上图中画出第5分钟到9分钟NH3浓度的变化曲线。____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com