
【题目】下列说法正确的是( )
A.3C(s)+CaC(s)?CaC2 (s)+CO(g)在常温下不能自发进行,说明该反应的△H>0
B.CH3COOH溶液加水稀释后,溶液中 ![]() 的值增大
的值增大
C.恒温恒压的密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)△H=﹣aKJ/mol,平衡时向容器中在充入一定量的NH3 , 重新达到平衡时a值不变
D.C(s)+H2O(g)?CO(g)+H2(g) (△H>0),其它条件不变时,升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法,化合物 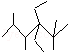 的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段 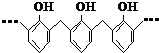 的高聚物,其单体是苯酚和甲醛
的高聚物,其单体是苯酚和甲醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可作为脱氯剂,已知25.0mL 0.200 mol·L-1的Na2S2O3溶液恰好把448mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32-将转化为( )
A. S2- B. S C. SO32- D. SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸某酯E的合成路线如图所示: 
已知:①2RCH2CHO ![]() R﹣
R﹣ ![]()
②A分子中只含有1个甲基;③D的相对分子质量为130;
(1)C中含氧官能团的名称为;反应④的反应方程式为;
(2)在合成路线中,设计⑤和⑦的目的;
(3)X是B的最简单同系物,请写出X与足量银氨溶液反应的离子方程式;
(4)下列有关说法正确的是;
a.B中有4种不同的氢
b.水杨酸与足量NaHCO3反应生成 ![]()
c.D不与金属钠反应
d.1mol E与氢气加成,最多消耗4mol H2
(5)H有多种同分异构体,其中能同时满足下列条件的共有种(不考虑立体异构)
①能发生银镜反应;②能发生水解反应;③能与FeCl3溶液发生显色反应,其中有5种氢,且氢的个数比为1:1:2:2:2的为(写结构简式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生甲设计了如下装置以验证亚硫酸与次氯酸的酸性强弱:H2SO3>HCl0。
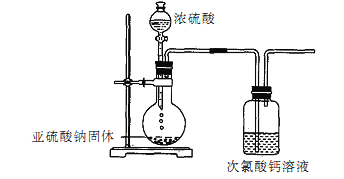
(1)甲得出结论的现象________________。
(2)学生乙对甲的实验结论提出了质疑,乙的理由是:____,随后对装置做了如下改进。

X、Y、Z是选用了下列部分试剂:饱和NaHC03溶液、品红溶液、NaOH溶液,乙得出结论的现象是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶质分子(或离子)和水分子结合成水合分子(水合离子)的过程是( )
A.物理过程,吸收热量B.化学过程,吸收热量
C.物理过程,放出热量D.化学过程,放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是登山运动员常用的能源提供剂.氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气,氢化钙在一定条件下与氧气反应生成的产物不只一种.氢化钙通常用氢气与金属钙加热制取,如图1是模拟制取装置. 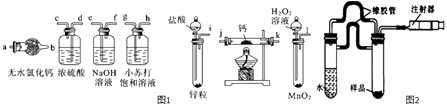
请回答下列问题:
(1)利用上述装置制取氢化钙时按气流方向连接顺序为(填仪器接口的字母编号).
i→→→→→→→a
(2)装有无水氯化钙装置的作用是 .
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(4)甲同学设计了一个实验,测定上述实验中得到的氢化钙的纯度.请完善下列实验步骤:
①样品称量;
②加入溶液(填化学式),搅拌;
③(填操作名称);洗涤;干燥
④称量碳酸钙.
(5)利用上述题目中给出的装置(试剂可另选)设计实验,用化学方法证明产物中含有氢化钙,写出实验简要步骤及观察到的现象 .
(6)乙同学利用图2所示装置测定上述实验中得到的氢化钙的纯度.他称取46mg所制得的氢化钙样品,记录开始时注射器活栓停留在lO.00mL刻度处,反应结束后充分冷却,活栓最终停留在57.04mL刻度处(上述气体体积均在标准状况下测定).试通过计算求样品中氢化钙的纯度: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、按要求书写下列反应的化学方程式或离子方程式:
(1)实验室制备氨气化学方程式_______________;
(2)工业制备漂白粉化学方程式_______________;
(3)二氧化硫与氧气反应化学方程式_______________;
(4)铝与氢氧化钠溶液反应的离子方程式_______________;
(5)磁性氧化铁与稀硝酸反应离子方程式_______________。
II.A~G 的转化关系如下图所示(部分反应物、产物和反应条件未标出)。

已知:①A、B 为中学化学常见的金属单质,C~G 均为化合物,并且E 和G均含有3 种元素; ②C 是淡黄色固休,D 既能与强酸溶液反应,又能与强碱溶液反应;③F 溶液中加入AgNO3溶液产生不溶于稀硝酸的白色沉淀; ④E 和G 焰色反应均呈黄色。
(1)写出下列物质D 的化学式______;
(2)①~⑥反应中,不属于氧化还原反应的是____________;
(3)将过量的E溶液逐滴加入F 溶液中,出现的现象是____________;
(4)F 和G 溶液混合可以生成白色胶状沉沉,反应的离子方程式为____________;
(5)反应③中,若有31.2gC 参加反应,转移电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2和SCl2均为重要的化工原料,都满足8电子稳定结构。
已知:①S2(1)+Cl2(g)![]() S2Cl2(g) △H1=xkJ/mol
S2Cl2(g) △H1=xkJ/mol
②S2Cl2(g)+Cl2(g)![]() 2SCl2(g) △H2=ykJ/mol
2SCl2(g) △H2=ykJ/mol
③相关化学键的键能如下表所示:
化学键 | S-S | S-Cl | Cl-Cl |
键能/kJ/mol | a | b | c |
下列说法错误的是
A. SCl2的结构式为C1-S-Cl B. S2Cl2的电子式为: ![]()
C. y=2b-a-c D. 在S2(1)+2Cl2(g)![]() 2SCl2(g)的反应中,△H=(x+y)kJ/mol
2SCl2(g)的反应中,△H=(x+y)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com