
下列说法正确的是
①泥浆中泥沙是溶质,水是溶剂
②医用酒精中,水是溶剂,酒精是溶质
③凡是分散质能通过半透膜的分散系即属于胶体
④胶体的聚沉属于物理过程
⑤通过丁达尔现象可以鉴别胶体和溶液
⑥胶体带电是电泳的前提条件
A.①②③④⑤ B.②④⑤ C.②③④⑤ D.②④⑤⑥
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源:2015-2016学年江苏省高二上学期期中选修化学试卷(解析版) 题型:选择题
在一定温度下的定容密闭容器中,当物质的下列物理量不再发生变化时,表明反应A(g)+2B(g) C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是
A.混合气体的密度 B.混合气体的总物质的量
C.混合气体的压强 D.混合气体的总体积
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中测试化学试卷(解析版) 题型:选择题
等体积等浓度的MOH强碱溶液和HA弱酸溶液混和,溶液中离子浓度关系不正确的是
A.c(M+)=c(HA)+c(A-) B.c(M+)>c(H+)>c(A-)>c(OH-)
C.c(OH-)=c(H+)+ c(HA) D.c(M+)+c(H+) =c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一10月月考化学试卷(解析版) 题型:选择题
下列溶液中,溶质的物质的量浓度为1 mol·L-1 的是
A.将80 g NaOH溶于2 L 水所得的溶液
B.将0.5 mol·L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液
C.将40 g NaOH 溶于水并配成1 L的溶液
D.含K+为4 mol·L-1的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源:2016届山西怀仁第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是
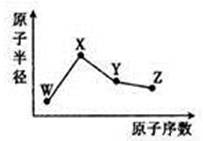
A.简单离子半径:W>X>Z
B.最简单气态氢化物的稳定性:Y<Z
C.化合物XZW中既含离子键又含共价键
D.Y的氧化物能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高二上期中考试化学试卷(解析版) 题型:实验题
实验室制备1,2-二溴乙烷的反应原理如下:

可能存在的主要副反应有:①乙醇在浓硫酸的存在下在l40℃脱水生成乙醚(CH3CH2OCH2CH3);②浓硫酸将乙醇脱水碳化。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | -1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____________;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入____________,其目的是吸收反应中可能生成的酸性气体:(填
正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是_____________________;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在______层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用________洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用_______________的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是____________;但又不能过度冷却(如用冰水),其原因是_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高二上期中考试化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关,下列说法不正确的是
A.为防止电池中的重金属元素污染土壤和水体,应积极开发废电池的综合利用技术
B.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
C.为了防止白色污染,应废止对塑料的研制和使用
D.石油的裂化可提高汽油等轻质油的质量和产量,裂解可得乙烯等
查看答案和解析>>
科目:高中化学 来源:2016届辽宁沈阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
研究化肥的合成、废水的处理等有现实的重要意义。
(1)工业生产中,以NH3为原料制硝酸,写出工业生产硝酸最后一步的化学方程式 。
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:

已知:CO+H2O CO2+H2;
CO2+H2;
按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。现有甲、乙、丙三家工厂生产原料如下:
甲厂以焦炭和水为原料;
乙厂以天然气和水为原料;
丙厂以石脑油(主要成分为C5H12)和水为原料。
请根据上述信息判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高:________(填“甲”、“乙”或“丙”)。
(3)将工厂废气中产生的SO2通过下列流程,可以转化为有应用价值的硫酸钙等。

①写出反应Ⅰ的化学方程式:_________________________________。
②生产中,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是_____________。
③检验经过反应Ⅲ得到的铵态氮肥中SO42-所用试剂是_______________________。
(4)为减少环境污染,工业上也常用Na2CO3溶液吸收制取HNO3产生的尾气中的NO2,生成NaNO3、NaNO2和一种气体,写出反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三12月月考化学试卷(解析版) 题型:填空题
用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。
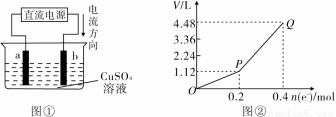
(1)电解过程中,a电极表面的现象是___________________________________;
(2)a电极上发生的反应为________________________________________________;
(3)从P点到Q点时收集到的混合气体的平均摩尔质量为___________ g·mol-1;
(4)如果要使溶液恢复到电解前的状态,向溶液中加入0.8 g CuO即可,则电解后溶液的pH为______;
(5)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com