
 æɼņŠ“ĪŖ
æɼņŠ“ĪŖ £®ĻÖӊij»ÆŗĻĪļWµÄ·Ö×Ó½į¹¹æɱķŹ¾ĪŖ£ŗ
£®ĻÖӊij»ÆŗĻĪļWµÄ·Ö×Ó½į¹¹æɱķŹ¾ĪŖ£ŗ £®
£® £®
£® ·ÖĪö £Ø1£©øł¾Ż½į¹¹¼ņŹ½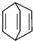 Š“³ö·Ö×ÓŹ½£»
Š“³ö·Ö×ÓŹ½£»
£Ø2£©øł¾Ż¶Ō³Ę½į¹¹ÅŠ¶ĻŅ»ĀČ“śĪļ£»
£Ø3£©øł¾ŻWµÄ½į¹¹¼ņŹ½ÅŠ¶ĻĖłŹōĄąŠĶ£¬×¢Ņā·¼ĻćĢžÖŠ±ŲŠėŗ¬ÓŠ±½»·£»
£Ø4£©øł¾ŻWŗ¬ÓŠµÄ¹ŁÄÜĶÅČ·¶ØĘäŠŌÖŹ£»
£Ø5£©WÓŠŅ»ÖÖ·¼Ļć×åµÄĶ¬·ÖŅģ¹¹Ģ壬ĖµĆ÷øĆĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ÓŠ±½»·£¬øĆĪļÖŹÄÜŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś¾ŪŗĻ·“Ó¦£¬ĖµĆ÷Ö§Į“ÉĻŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£®
½ā“š ½ā£ŗ£Ø1£©øł¾ŻWµÄ½į¹¹¼ņŹ½ ÖŖ£¬WµÄ·Ö×ÓŹ½ĪŖ£ŗC8H8£¬¹Ź“š°øĪŖ£ŗC8H8£»
ÖŖ£¬WµÄ·Ö×ÓŹ½ĪŖ£ŗC8H8£¬¹Ź“š°øĪŖ£ŗC8H8£»
£Ø2£©W ĪŖŹĒ¶Ō³Ę½į¹¹£¬øĆ»ÆŗĻĪļÖŠÖ»ÓŠĮ½ĄąĒāŌ×Ó£¬ĖłŅŌĘäŅ»ĀČ“śĪļÓŠ2ÖÖ£¬¹Ź“š°øĪŖ£ŗ2£»
ĪŖŹĒ¶Ō³Ę½į¹¹£¬øĆ»ÆŗĻĪļÖŠÖ»ÓŠĮ½ĄąĒāŌ×Ó£¬ĖłŅŌĘäŅ»ĀČ“śĪļÓŠ2ÖÖ£¬¹Ź“š°øĪŖ£ŗ2£»
£Ø3£©a£®W֊ƻӊ±½»·£¬ĖłŅŌ²»ŹōÓŚ·¼ĻćĢž£¬¹Źa“ķĪó£»
b£®WŹĒ»·×“Ģ¼Ēā»ÆŗĻĪļ£¬ĒŅ²»ŗ¬±½»·£¬ĖłŅŌŹōÓŚ»·Ģž£¬¹ŹbÕżČ·£»
c£®WÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĖłŅŌŹōÓŚ²»±„ŗĶĢž£¬¹ŹcÕżČ·£»
d£®WÖŠ²»ŗ¬Ģ¼Ģ¼Čż¼ü£¬ĖłŅŌ²»ŹōÓŚČ²Ģž£¬¹Źd“ķĪó£»
¹ŹŃ”bc£»
£Ø4£©a£®ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ÄÜŗĶĒāĘų·¢Éś¼Ó³É·“Ó¦£¬¼“ÄÜ·¢Éś»¹Ō·“Ó¦£¬¹ŹaÕżČ·£»
b£®WŹōÓŚĢ¼Ēā»ÆŗĻĪļ£¬ÄÜČ¼ÉÕ£¬ĖłŅŌÄÜ·¢ÉśŃõ»Æ·“Ó¦£¬¹ŹbÕżČ·£»
c£®W·Ö×ÓÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ÄÜ·¢Éś¼Ó¾Ū·“Ó¦£¬¹ŹcÕżČ·£»
d£®±½µÄ·Ö×ÓŹ½ĪŖC6H6£¬WµÄ·Ö×ÓŹ½ĪŖ£ŗC8H8£¬Ęä×ī¼ņŹ½ĻąĶ¬£¬ĖłŅŌµČÖŹĮæµÄWÓė±½·Ö±šĶźČ«Č¼ÉÕ£¬¶žÕßĻūŗĵÄŃõĘųĻąĶ¬£¬¹Źd“ķĪó£»
¹ŹŃ”d£»
£Ø5£©WÓŠŅ»ÖÖ·¼Ļć×åµÄĶ¬·ÖŅģ¹¹Ģ壬ĖµĆ÷øĆĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ÓŠ±½»·£¬øĆĪļÖŹÄÜŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś¾ŪŗĻ·“Ó¦£¬ĖµĆ÷Ö§Į“ÉĻŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬øł¾ŻWµÄ·Ö×ÓŹ½ÖŖ£¬øĆĶ¬·ÖŅģ¹¹ĢåĪŖ±½ŅŅĻ©£¬±½ŅŅĻ©·¢Éś¼Ó¾Ū·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹ£¬ĢāÄæÄѶČÖŠµČ£¬øł¾ŻÓŠ»śĪļµÄ¹ŁÄÜĶÅĄ“Č·¶ØĘäŠŌÖŹ£¬×¢Ņā·¼ĻćĢžŗĶ»·ĢžµÄĒų±š£¬ŅדķŃ”ĻīŹĒ£Ø4£©D£¬øł¾ŻĘä×ī¼ņŹ½Č·¶ØŠčŅŖŃõĘųµÄĮ棬ĪŖŅדķµć£®


 ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓČČæɼų±šĢ¼ĖįĒāÄĘÓėĢ¼ĖįÄĘ | |
| B£® | ŃęÉ«·“Ó¦æɼų±š¼ŲŃĪŗĶÄĘŃĪ | |
| C£® | ÓĆĖ®æɼų±šĒāŃõ»ÆĆ¾ŗĶĒāŃõ»ÆĀĮ¹ĢĢå | |
| D£® | KSCNČÜŅŗæɼų±šFe3+ÓėFe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖæÉÄę·“Ó¦A£Øg£©+B£Øg£©?C£Øg£©+D£Øg£©¹ż³ĢÖŠµÄÄÜĮæ£ØkJ£©±ä»ÆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
ŅŃÖŖæÉÄę·“Ó¦A£Øg£©+B£Øg£©?C£Øg£©+D£Øg£©¹ż³ĢÖŠµÄÄÜĮæ£ØkJ£©±ä»ÆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĖ®ŗĶµā»Æ¼Ų·“Ó¦£ŗCl2+2I-=2Cl-+I2 | |
| B£® | ¶žŃõ»ÆĆĢŗĶŃĪĖįÖĘĀČĘų£ŗMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++2H2O+Cl2”ü | |
| C£® | ĀČĘųÖĘĘÆ°×·Ū£ŗ2OH-+Cl2=Cl-+Cl0-+H2O | |
| D£® | ĀČĘųŗĶĖ®·“Ó¦£ŗCl2+H2O=H++Cl-+HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŚ°ĖÖÜĘŚ¢óA×å | B£® | µŚĮłÖÜĘŚ¢õA×å | C£® | µŚĘßÖÜĘŚ¢ōB×å | D£® | µŚĘßÖÜĘŚ¢ōA×å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijæĪĶāŠ”×éµÄĶ¬Ń§ÄāÓĆ·ĻĀĮ²ÖĘČ”ĮņĖįĀĮ¾§Ģ壬ŅŃÖŖĀĮµÄĪļÖÖĄą±šÓėČÜŅŗpH¹ŲĻµČēĶ¼ĖłŹ¾£®
ijæĪĶāŠ”×éµÄĶ¬Ń§ÄāÓĆ·ĻĀĮ²ÖĘČ”ĮņĖįĀĮ¾§Ģ壬ŅŃÖŖĀĮµÄĪļÖÖĄą±šÓėČÜŅŗpH¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6.4gÓÉO3ŗĶO2×é³ÉµÄ»ģŗĻĘųĢåÖŠŅ»¶Øŗ¬ÓŠ0.4NAøöŌ×Ó | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬5.6gĢś·ŪŌŚ7.1gĀČĘųÖŠ³ä·ÖČ¼ÉÕ£¬Ź§Č„µÄµē×ÓŹżÄæĪŖ0.3NA | |
| C£® | ³£ĪĀĻĀ£¬pH=1µÄHNO3ČÜŅŗÖŠŗ¬ÓŠ0.1NAøöH+ | |
| D£® | 0.1mol KHSO4¾§ĢåÖŠŗ¬ÓŠµÄŃōĄė×ÓŹżŹĒ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| 1 | 2 | 3 | |
| æÕ°×ŹµŃéĻūŗÄĮņĖįīę±ź×¼ČÜŅŗµÄĢå»ż£Øml£© | 0.75 | 0.50 | 0.80 |
| 0.25æĖѳʷĻūŗÄĮņĖįīę±ź×¼ČÜŅŗµÄĢå»ż£Øml£© | 24.65 | 24.75 | 24.70 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µČĪļÖŹµÄĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöµÄČČĮæÉŁ | |
| B£® | Óɵ„ÖŹA×Ŗ»ÆĪŖµ„ÖŹBŹ±”÷H=+119 kJ•mol-1æÉÖŖµ„ÖŹB±Čµ„ÖŹAĪČ¶Ø | |
| C£® | Ļ”ČÜŅŗÖŠ£ŗH+£Øaq£©+OH-£Øaq£©ØTH2O£Øl£©”÷H=-57.3 kJ•mol-1£¬Čō½«ŗ¬0.5 mol H2SO4µÄÅØĮņĖįÓėŗ¬1 mol NaOHµÄČÜŅŗ»ģŗĻ£¬·Å³öµÄČČĮæŠ”ÓŚ57.3 kJ | |
| D£® | ŌŚ101 kPaŹ±£¬H2Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ĪŖ2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-571.6 kJ•mol-1£¬ŌņH2ŌŚ101 kPaŹ±µÄČ¼ÉÕČČĪŖ571.6 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com