
ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠČēĻĀŹµŃé:
(1)ŌŚ¼ģ²é×°ÖƵÄĘųĆÜŠŌŗó,ĻņŹŌ¹ÜaÖŠ¼ÓČė10 mL 6 mol”¤L-1µÄĻ”ĻõĖįŗĶ1 gĶʬ,Į¢¼“ÓĆ“ųÓŠµ¼¹ÜµÄĻšĘ¤ČūČū½ōŹŌ¹ÜæŚ”£ĒėŠ“³öŌŚŹŌ¹ÜaÖŠÓŠæÉÄÜ·¢ÉśµÄĖłÓŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½”””£
(2)ŌŚŹµŃé¹ż³ĢÖŠ³£³£·“Ó¦æŖŹ¼Ź±ĖŁĀŹ»ŗĀż,ĖęŗóÖš½„¼Óæģ,ÕāŹĒÓÉÓŚ””””””””””””””””””””,µ±·“Ó¦½ųŠŠŅ»¶ĪŹ±¼äŗóĖŁĀŹÓÖÖš½„¼õĀż,ŌŅņŹĒ”””£
(3)Óū½ĻæģµŲÖʵĆNO,æɲÉČ”µÄ“ėŹ©ŹĒ””””””(ĢīŠ“×ÖÄøŠņŗÅ)”£
| A£®¼ÓČČ | B£®Ź¹ÓĆĶ·Ū | C£®Ļ”ŹĶHNO3 | D£®Ōö“óĻõĖįµÄÅØ¶Č |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚČܼĮĪŖ1LµÄĆܱÕČŻĘ÷ÄŚ·ÅČė2molN2O4ŗĶ8molNO2£¬·¢ÉśČēĻĀ·“Ó¦2 NO2(ŗģ×ŲÉ«) N2O4(ĪŽÉ«) ”÷H£¼0·“Ó¦ÖŠNO2”¢N2O4µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼£¬°“ĻĀĮŠŅŖĒó×÷“š£ŗ
N2O4(ĪŽÉ«) ”÷H£¼0·“Ó¦ÖŠNO2”¢N2O4µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼£¬°“ĻĀĮŠŅŖĒó×÷“š£ŗ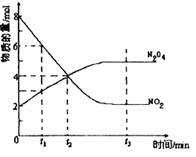
£Ø1£©ŌŚøĆĪĀ¶ČĻĀ£¬·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ£ŗ ”£
£Ø2£©Čōt1£½10s£¬t2£½20s£¬¼ĘĖć“Ót1ÖĮt2Ź±ŅŌN2O4±ķŹ¾µÄ·“Ó¦ĖŁĀŹ£ŗ mol”¤ L-1”¤ s-1”£
£Ø3£©Ķ¼ÖŠt1”¢t2”¢t3ÄÄŅ»øöŹ±æĢ±ķŹ¾·“Ó¦ŅŃ¾“ļµ½Ę½ŗā£æ“š£ŗ ”£
£Ø4£©t1Ź±£¬Õż·“Ó¦ĖŁĀŹ £ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©Äę·“Ó¦ĖŁĀŹ”£
£Ø5£©Ī¬³ÖČŻĘ÷µÄĪĀ¶Č²»±ä£¬ČōĖõŠ”ČŻĘ÷µÄĢå»ż£¬ŌņĘ½ŗāĻņ ŅĘ¶Æ£ØĢī”°Õż·“Ó¦·½Ļņ”±”¢”°Äę·“Ó¦·½Ļņ”±»ņ”°²»±ä”±£©
£Ø6£©Ī¬³ÖČŻĘ÷µÄĢå»ż²»±ä£¬ÉżøßĪĀ¶Č£¬“ļµ½ŠĀĘ½ŗāŹ±ĢåĻµµÄŃÕÉ« £ØĢī”°±äÉī”±”¢”°±äĒ³”±»ņ”°²»±ä”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(6 ·Ö)¶ž¼×ĆŃŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąČ¼ĮĻ£¬æÉŅŌĶعżCH3OH·Ö×Ó¼äĶŃĖ®ÖĘµĆ£ŗ2CH3OH(g) CH3OCH3(g)£«H2O(g) ¦¤H£½£23.5 kJ”¤mol£1”£ŌŚT1”ę£¬ŗćČŻĆܱÕČŻĘ÷ÖŠ½ØĮ¢ÉĻŹöĘ½ŗā£¬ĢåĻµÖŠø÷×é·ÖÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OCH3(g)£«H2O(g) ¦¤H£½£23.5 kJ”¤mol£1”£ŌŚT1”ę£¬ŗćČŻĆܱÕČŻĘ÷ÖŠ½ØĮ¢ÉĻŹöĘ½ŗā£¬ĢåĻµÖŠø÷×é·ÖÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
(1)øĆĢõ¼žĻĀ·“Ó¦Ę½ŗā³£Źż±ķ“ļŹ½K£½________”£ŌŚT1”ꏱ£¬·“Ó¦µÄĘ½ŗā³£ŹżĪŖ________£»
(2)ĻąĶ¬Ģõ¼žĻĀ£¬ČōøıäĘšŹ¼ÅØ¶Č£¬Ä³Ź±æĢø÷×é·ÖÅضČŅĄ“ĪĪŖc(CH3OH)£½0.4 mol”¤L£1£¬c(H2O)£½0.6 mol”¤L£1”¢c(CH3OCH3)£½1.2 mol”¤L£1£¬“ĖŹ±Õż”¢Äę·“Ó¦ĖŁĀŹµÄ“󊔣ŗv(Õż)________v(Äę)(Ģī”°>”±”¢”°<”±»ņ”°£½”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ČÜŅŗÖŠ£¬·“Ó¦A£«2B C·Ö±šŌŚČżÖÖ²»Ķ¬ŹµŃéĢõ¼žĻĀ½ųŠŠ£¬ĖüĆĒµÄĘšŹ¼ÅØ¶Č¾łĪŖc(A)
C·Ö±šŌŚČżÖÖ²»Ķ¬ŹµŃéĢõ¼žĻĀ½ųŠŠ£¬ĖüĆĒµÄĘšŹ¼ÅØ¶Č¾łĪŖc(A)
£½0.100 mol/L”¢c(B)£½0.200 mol/L¼°c(C)£½0 mol/L”£·“Ó¦ĪļAµÄÅضČĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾”£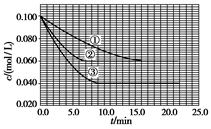
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Óė¢Ł±Č½Ļ£¬¢ŚŗĶ¢Ū·Ö±š½öøıäŅ»ÖÖ·“Ó¦Ģõ¼ž”£ĖłøıäµÄĢõ¼žŗĶÅŠ¶ĻµÄĄķÓÉŹĒ£ŗ
¢Ś £»
¢Ū ”£
(2)ŹµŃé¢ŚĘ½ŗāŹ±BµÄ×Ŗ»ÆĀŹĪŖ £»ŹµŃé¢ŪĘ½ŗāŹ±CµÄÅضČĪŖ ”£
(3)øĆ·“Ó¦µÄ¦¤H 0£¬ĘäÅŠ¶ĻĄķÓÉŹĒ ”£
(4)øĆ·“Ó¦½ųŠŠµ½4.0 minŹ±µÄĘ½¾ł·“Ó¦ĖŁĀŹ£ŗ
ŹµŃé¢Ś£ŗv(B)£½ ”£
ŹµŃé¢Ū£ŗv(C)£½ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ijĪĀ¶ČŹ±ŌŚ2LČŻĘ÷ÖŠX”¢Y”¢ZČżÖÖĘųĢ¬ĪļÖŹµÄĪļÖŹµÄĮæ£Øn£©Ėꏱ¼ä£Øt£©±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ÓÉĶ¼ÖŠŹż¾Ż·ÖĪö£ŗ
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
£Ø2£©·“Ó¦æŖŹ¼ÖĮ2min£¬ÓĆX±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ£ŗ
£Ø3£©ĻĀĮŠŠšŹöÄÜĖµĆ÷ÉĻŹö·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ £ØĢī×ÖÄø£©
A£®»ģŗĻĘųĢåµÄ×ÜĪļÖŹµÄĮæ²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»Æ
B£®µ„Ī»Ź±¼äÄŚĆæĻūŗÄ3mol X£¬Ķ¬Ź±Éś³É2mol Z
C£®»ģŗĻĘųĢåµÄ×ÜÖŹĮæ²»Ėꏱ¼äµÄ±ä»Æ¶ų±ä»Æ
£Ø4£©ŌŚĆܱÕČŻĘ÷Ąļ£¬ĶØČėa mol X(g)ŗĶb mol Y(g)£¬·¢Éś·“Ó¦X(g£©+ Y(g£©=2Z(g)£¬µ±øıäĻĀĮŠĢõ¼žŹ±£¬·“Ó¦ĖŁĀŹ»į·¢ÉśŹ²Ć“±ä»Æ£ØŃ”Ģī”°Ōö“ó”±”¢”° ¼õŠ””± »ņ”°²»±ä”±£©
¢Ł ½µµĶĪĀ¶Č£ŗ
¢Ś±£³ÖČŻĘ÷µÄĢå»ż²»±ä£¬Ōö¼ÓX(g)µÄĪļÖŹµÄĮæ£ŗ
¢Ū Ōö“óČŻĘ÷µÄĢå»ż£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ÓÉÓŚĪĀŹŅŠ§Ó¦ŗĶ׏Ō“¶ĢȱµČĪŹĢā£¬ČēŗĪ½µµĶ“óĘųÖŠµÄCO2ŗ¬Įæ²¢¼ÓŅŌæŖ·¢ĄūÓĆ£¬ŅżĘšĮĖø÷½ēµÄĘÕ±éÖŲŹÓ”£ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆCO2Éś²śČ¼ĮĻ¼×“¼”£Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2(g)£«3H2(g) CH3OH(g)£«H2O(g)£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ
CH3OH(g)£«H2O(g)£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ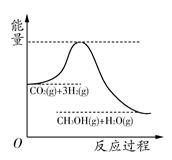
(1)ÉĻŹö·“Ó¦Ę½ŗā³£ŹżKµÄ±ķ“ļŹ½ĪŖ________£¬ĪĀ¶Č½µµĶ£¬Ę½ŗā³£ŹżK________(Ģī”°Ōö“ó”±”¢”°²»±ä”±»ņ”°¼õŠ””±)”£
(2)ŌŚĢå»żĪŖ2 LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė1 mol CO2ŗĶ3 mol H2£¬²āµĆCO2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĻĀ±ķĖłŹ¾”£“Ó·“Ó¦æŖŹ¼µ½5 minÄ©£¬ÓĆĒāĘųÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½________”£
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
½«10 mol AŗĶ5 mol B·ÅČėČŻ»żĪŖ10 LµÄĆܱÕČŻĘ÷ÖŠ,ijĪĀ¶ČĻĀ·¢Éś·“Ó¦:3A(g)+B(g) 2C(g),ŌŚ×ī³õ2 sÄŚ,ĻūŗÄAµÄĘ½¾łĖŁĀŹĪŖ0.06 mol”¤L-1”¤s-1,ŌņŌŚ2 sŹ±,ČŻĘ÷ÖŠÓŠ mol A,“ĖŹ±CµÄĪļÖŹµÄĮæÅضČĪŖ ”£
2C(g),ŌŚ×ī³õ2 sÄŚ,ĻūŗÄAµÄĘ½¾łĖŁĀŹĪŖ0.06 mol”¤L-1”¤s-1,ŌņŌŚ2 sŹ±,ČŻĘ÷ÖŠÓŠ mol A,“ĖŹ±CµÄĪļÖŹµÄĮæÅضČĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(““ŠĀŌ¤²āĢā)(1)ŌŚ100 ”ęŗćĪĀĢõ¼žĻĀ½«0.100 molµÄN2O4³äČėĢå»żĪŖ1 LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗN2O4(g) 2NO2(g)””¦¤H£¾0”£øōŅ»¶ØŹ±¼ä¶ŌøĆČŻĘ÷ÄŚµÄĪļÖŹ½ųŠŠ·ÖĪö£¬µĆµ½ČēĻĀŹż¾Ż£ŗ
2NO2(g)””¦¤H£¾0”£øōŅ»¶ØŹ±¼ä¶ŌøĆČŻĘ÷ÄŚµÄĪļÖŹ½ųŠŠ·ÖĪö£¬µĆµ½ČēĻĀŹż¾Ż£ŗ
| ””t/s c/(mol”¤L£1)”””” | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol”¤L£1) | 0.100 | a | 0.5b | 0.4b | | |
| c(NO2)/(mol”¤L£1) | 0 | 0.060 | b | c1 | c2 | c3 |
 H4SiO4(aq)””¦¤H
H4SiO4(aq)””¦¤H²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©Ä³ŗćĪĀŗćČŻĢõ¼žĻĀµÄæÉÄę·“Ó¦£ŗN2(g)+3H2(g)  2NH3(g) ”÷H£¼0£¬ĘšŹ¼ ³äČė£įmol N2”¢£āmol H2£¬ “ļµ½Ę½ŗāŗó£¬N2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ1 mol”¢3 mol”¢10 mol£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
2NH3(g) ”÷H£¼0£¬ĘšŹ¼ ³äČė£įmol N2”¢£āmol H2£¬ “ļµ½Ę½ŗāŗó£¬N2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ1 mol”¢3 mol”¢10 mol£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁA= £¬ B= £»
¢Ś Ę½ŗāŗó£¬ŌŁ³äČė5 molNH3£¬»ÆŃ§Ę½ŗā½«Ļņ ŅĘ¶Æ£ØĢī”°×ó”±»ņ”°ÓŅ”±»ņ”°²»ŅĘ¶Æ”±£©£¬“ļŠĀĘ½ŗāŹ±N2µÄ°Ł·Öŗ¬Įæ ŌĘ½ŗāŹ±N2µÄ°Ł·Öŗ¬Įæ£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©£»
¢ŪĘ½ŗāŗóČōÉżøßĪĀ¶Č£¬ŌņĘ½ŗāĻņ ·½ĻņŅĘ¶Æ£»ČōŌö¼ÓŃ¹Ē棬ŌņĘ½ŗāĻņ
·½ĻņŅĘ¶Æ£ØĢī”°Ļņ×ó”±»ņ”°ĻņÓŅ”±£©”£
£Ø2£©Ä³ŗćĪĀŗćŃ¹Ģõ¼žĻĀµÄæÉÄę·“Ó¦£ŗN2(g)+3H2(g)  2NH3(g)£¬ĘšŹ¼³äČė1 mol N2”¢3 mol H2”¢16 mol NH3£¬ČŻĘ÷µÄČŻ»żĪŖV L”£“ļµ½Ę½ŗāŗó£¬N2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖAmol”¢Bmol”¢c mol£¬“ĖŹ±ČŻĘ÷µÄČŻ»żĪŖ1.1V L£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
2NH3(g)£¬ĘšŹ¼³äČė1 mol N2”¢3 mol H2”¢16 mol NH3£¬ČŻĘ÷µÄČŻ»żĪŖV L”£“ļµ½Ę½ŗāŗó£¬N2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖAmol”¢Bmol”¢c mol£¬“ĖŹ±ČŻĘ÷µÄČŻ»żĪŖ1.1V L£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
¢Ł ĘšŹ¼Ź±·“Ó¦ĖŁĀŹVÕż VÄę£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©
¢Ś Ę½ŗāŹ±A= £¬B= ”£
¢Ū ČōĘ½ŗāŗóŌŁ³äČė3.6 molNH3£¬ÖŲŠĀ½ØĮ¢Ę½ŗāŹ±ČŻĘ÷µÄČŻ»żĪŖ L”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com