
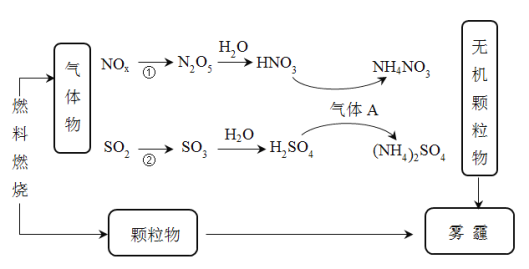
【题目】研究表明,氮氧化物和二氧化硫等气体与雾霾的形成有关(如图所示)。
(1)过程①中NOx(x=1或2)发生_______(填“氧化”或“还原”)反应。
(2)气体A的化学式是________。
(3)过程②的化学方程式是________。
(4)已知:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H1= -a kJ/mol
S(s)+O2(g)=SO2(g) △H2= -b kJ/mol
家庭常用燃料液化石油气中含有微量H2S,在燃烧过程中会产生SO2。该反应的热化学方程式是____________。
【答案】氧化 NH3 2SO2+O2![]() 2SO3 2H2S(g)+3O2(g) == 2SO2(g)+2H2O(l) △H= -(a+2b) kJ/mol
2SO3 2H2S(g)+3O2(g) == 2SO2(g)+2H2O(l) △H= -(a+2b) kJ/mol
【解析】
由图可知:燃料产生的氮氧化物转化成最高价氮的氧化物,并和水反应生成硝酸,进一步与NH3生成铵盐;产生的二氧化硫转化成最高价硫的氧化物SO3,并与水形成硫酸,进一步与氨气生成硫酸铵;两种铵盐和燃料燃烧产生的颗粒物形成雾霾。在此认识基础上对本题做出解答。
(1)NO或NO2生成N2O5,N化合价升高,被氧化,发生氧化反应,故答案为:氧化
(2)与HNO3或H2SO4反应生成相应铵盐的气体是NH3,故答案为:NH3
(3)SO2生成SO3需要在催化剂作用下发生:2SO2+O2![]() 2SO3,故答案为:2SO2+O2
2SO3,故答案为:2SO2+O2![]() 2SO3
2SO3
(4)由反应:2H2S(g)+O2(g)=2S(s)+2H2O(l) ①S(s)+O2(g)=SO2(g)②,由盖斯定律可知①+2×②得到H2S燃烧生成SO2的反应:2H2S(g)+3O2(g) =2SO2(g)+2H2O(l) △H,故△H=△H1+2△H2=-(a+2b) kJ/mol,则该反应的热化学方程式为:2H2S(g)+3O2(g) =2SO2(g)+2H2O(l) △H =-(a+2b) kJ/mol,故答案为:2H2S(g)+3O2(g) = 2SO2(g) + 2H2O(l) △H =-(a+2b) kJ/mol


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】电导率可用于衡量电解质溶液导电能力的大小。室温下,用0.100 mol·L-1 NH3·H2O滴定10 mL浓度均为0.100 mol·L-1HCl和CH3COOH的混合液,电导率曲线如图所示。

下列说法正确的是
A.①溶液中c(H+)为0.200 mol·L-1
B.溶液温度高低为①>③>②
C.③点溶液中有c(Cl-)>c(CH3COO-)
D.③点后因离子数目减少使电导率略降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:配制50 mL 0.001 mol/L FeCl3溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴1 mol/L HCl溶液、1滴1 mol/L NaOH 溶液,测得溶液pH随时间变化的曲线如下图所示。
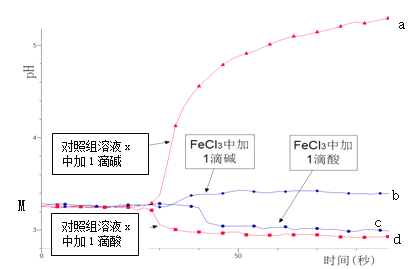
下列说法不正确的是
A.依据M点对应的pH,说明Fe3+发生了水解反应
B.对照组溶液x的组成可能是0.003 mol/L KCl
C.依据曲线c和d说明Fe3+水解平衡发生了移动
D.通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.0.1mol/L氨水中滴入等浓度等体积的醋酸,溶液导电性增强
B.适当升高温度,CH3COOH溶液pH增大
C.稀释0.1 mol/L NaOH溶液,水的电离程度减小
D.CH3COONa溶液中加入少量CH3COOH,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx(主要成分为NO、NO2的混合物),对烟气进行脱硫、脱硝有多种方法。
(1)碱液吸收法:采用石灰乳脱除SO2.脱除后的主要产物是_____。
(2)液相氧化法:采用 NaClO溶液进行脱除。
①NaClO水解的离子方程式是_____。
②NaClO溶液吸收NO的主要过程如下
i.NO(aq)+HClO(aq)NO2(aq)+HCl(aq) △H1
ii.3NO2(aq)+H2O(1)2HNO3(aq)+NO(aq) △H2
NO(aq)转化为HNO3(aq)的热化学方程式是_____。
③研究pH对NO脱除率的影响。调节 NaClO溶液的初始pH,NO的脱除率如表:
初始pH | 3.5 | 4.5 | 5.5 | 6.5 | 7.5 |
NO脱除率 | 91% | 88% | 83% | 65% | 51% |
pH影响NO脱除率的原因是_____。
(3)研究发现,在液相氧化法中,一定量的SO2能提高NOx的脱除率。当pH=5.5时,SO2对有效氯含量、NOx脱除率的影响如图所示。

①据图1,通入SO2后有效氯含量降低。SO2和HClO反应的离子方程式是_____。
②针对图2中NOx脱除率提高的原因,研究者提出了几种可能发生的反应:
A.SO2+2NO+H2O═N2O+H2SO4
B.2SO2+2NO+2H2O═N2+2H2SO4
C.4SO2+2NO2+4H2O═N2+4H2SO4
用同位素示踪法确认发生的反应:把15NO2和NO按一定比例混合,通入SO2的水溶液中,检测气体产物。
a.气体产物中主要含有15NO2、N2O,则发生的主要反应是_____(填序号)。
b.同时检测到气体产物中还有15N N,产生15N N的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________。
a.Fe(NO3)27H2O和Fe(NO3)24H2O
b.Fe(NO3)27H2O和Fe(NO3)2H2O
c.Fe(NO3)24H2O和Fe(NO3)2H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯化铁水溶液呈___性,原因是(用离子方程式表示):___;把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是___;热的纯碱溶液去油污能力强,纯碱水解的离子方程式为___(写第一步即可)。
(2)普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是___。
(3)已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为0.1mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)___;
④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2=4NO+6H2O,若反应速率分别用ν(NH3)、ν(O2)、ν(NO)、ν(H2O)[摩/(升分)]表示,则不正确的关系是( )
A.![]() ν(NH3)=ν(O2)B.
ν(NH3)=ν(O2)B.![]() ν(O2)=ν(H2O)
ν(O2)=ν(H2O)
C.![]() ν(NH3)=ν(H2O)D.
ν(NH3)=ν(H2O)D.![]() ν(O2)=ν(NO)
ν(O2)=ν(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com