
【题目】盐酸阿比多尔是一种盐酸盐,其主要作用是通过抑制流感病毒脂膜与宿主细胞的融合而阻断病毒的复制,结构如图。回答下列问题:
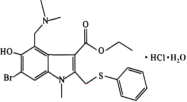
(1)盐酸阿比多尔中所含N、O、S三种元素第一电离能由大到小的顺序为___。O原子核外有___种不同运动状态的电子,基态S原子的价电子排布图不是![]() ,是因为该排布方式违背了___。
,是因为该排布方式违背了___。
(2)该结构中N原子的杂化方式是___。已知在氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°,分析原因为___。
(3)盐酸阿比多尔中不含有的化学键类型为___(填选项字母)。
A.离子键 B.配位键 C.金属键 D.σ键 E.π键 F.极性键 G.非极性键
(4)以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。GaN晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图。
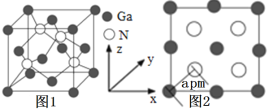
①氮化硼与氮化镓的结构类似,氮化硼熔点3000℃,氮化镓熔点1700℃,分析它们熔点不同的原因____。
②晶胞中与一个Ga原子距离最近且相等的N原子有____个。
③设阿伏加德罗常数的值为NA,则该晶胞的密度是___g·cm3(列出计算表达式)。
【答案】N>O>S 8 洪特规则 sp3、sp2 氨分子与Zn2+形成配合物后,孤对电子与Zn2+成键,原孤对电子与成键电子对之间的排斥作用变为成键电子对之间的排斥作用,排斥作用减弱,所以H—N—H键角变大 C 氮化硼和氮化镓都是共价晶体,B—N键长比Ga—N键长短,键能大,熔点高 4 ![]()
【解析】
(1)同周期元素从左至右第一电离能呈逐渐增大的趋势,同主族元素从上到下第一电离能呈逐渐减小的趋势,N原子最外层电子排布为半充满状态,处于稳定状态,第一电离能比同周期相邻元素大,则N、O、S三种元素第一电离能由大到小的顺序为N>O>S;O原子核外有8个电子,每个电子的运动状态都不同,则不同运动状态的电子有8种;洪特规则规定电子分布到能量简并的原子轨道时,优先以自旋相同的方式分别占据不同的轨道,因为这种排布方式原子的总能量最低,则基态S原子的价电子排布图![]() 违反了洪特规则;
违反了洪特规则;
(2)盐酸阿比多尔分子结构中含有2个N原子,分别如图标注所示: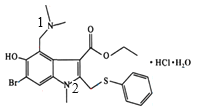 ,1号氮原子与三个碳原子形成碳氮单键,类似于氨分子的空间结构,该氮原子为sp3杂化,2号氮原子与碳碳双键直接相连,与碳碳双键形成平面结构,该氮原子的空间构型为平面三角形,为sp2杂化;氨分子与Zn2+结合变为[Zn(NH3)6]2+时,孤电子对变为成键电子对,原孤对电子与成键电子对之间的排斥作用变为成键电子对之间的排斥作用,排斥作用减弱,所以H—N—H键角变大,因此氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°;
,1号氮原子与三个碳原子形成碳氮单键,类似于氨分子的空间结构,该氮原子为sp3杂化,2号氮原子与碳碳双键直接相连,与碳碳双键形成平面结构,该氮原子的空间构型为平面三角形,为sp2杂化;氨分子与Zn2+结合变为[Zn(NH3)6]2+时,孤电子对变为成键电子对,原孤对电子与成键电子对之间的排斥作用变为成键电子对之间的排斥作用,排斥作用减弱,所以H—N—H键角变大,因此氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°;
(3)盐酸阿比多尔是一种盐酸盐,属于离子化合物,含有离子键;类比铵盐的形成,氨基中氮原子与HCl中的氢离子形成配位键;根据结构图所示,结构中含有多条不同的单键,单键都为σ键,分子结构中含有苯环和碳氧双键,苯环中含有离域大π键,碳氧双键中一个σ键和一个π键;氢氧单键为不同非金属元素形成的共价键,为极性共价键,碳碳键由同种元素形成的共价键,为非极性共价键,金属键为金属晶体中特有的键,该盐中不含金属键,答案选C;
(4)①氮化硼和氮化镓都是共价晶体,B—N键长比Ga—N键长短,键能大,熔点高;
②以该晶胞中面心上的Ga为中心,与该Ga原子距离最近且相等的N原子有2个,该晶胞上方无隙并置一个相同的晶胞,还有两个与该Ga原子距离最近且相等的N原子,则共有4个;
③根据图1所示,Ga位于晶胞的顶点和面心,Ga原子的数目为![]() ×8+6×
×8+6×![]() =4个,N位于晶胞的体内,N原子的个数为4个,则一个晶胞中含有4个氮化镓(GaN),晶胞的质量为
=4个,N位于晶胞的体内,N原子的个数为4个,则一个晶胞中含有4个氮化镓(GaN),晶胞的质量为![]() ,根据图2所示,晶胞的面对角线长度为4apm=4a×10-10cm,则晶胞的边长为,则晶胞的体积为(2
,根据图2所示,晶胞的面对角线长度为4apm=4a×10-10cm,则晶胞的边长为,则晶胞的体积为(2![]() a×10-10)3 cm3,根据晶胞密度计算公式ρ=
a×10-10)3 cm3,根据晶胞密度计算公式ρ= =
=![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】取1 mL 0.1 mol·L-1 AgNO3溶液进行如下实验(实验中所用试剂浓度均为0.1 mol·L-1):

下列说法不正确的是
A. 实验①白色沉淀是难溶的AgCl B. 由实验②说明AgI比AgCl更难溶
C. 若按①③顺序实验,看不到黑色沉淀 D. 若按②①顺序实验,看不到白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法匹拉韦(Favipiravir)是一种RNA聚合酶抑制剂,被用于治疗新型和复发型流感,主要通过阻断病毒核酸复制的方法抑制病毒增殖,其结构如图。下列关于法匹拉韦的说法错误的是( )
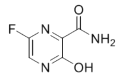
A.分子式为C5H4FN3O2
B.所有原子可能在同一平面上
C.所有碳原子的杂化方式都是sp2杂化
D.一定条件下能与氢氧化钠溶液、盐酸、氢气等发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4酸性溶液处理硫化亚铜(Cu2S)和二硫化亚铁(FeS2)的混合物时,发生的反应Ⅰ:![]() +Cu2S+H+→Cu2++
+Cu2S+H+→Cu2++![]() +Mn2++H2O(未配平)和反应Ⅱ:
+Mn2++H2O(未配平)和反应Ⅱ:![]() +FeS2+H+→Fe3++
+FeS2+H+→Fe3++![]() +Mn2++H2O(未配平)。下列说法正确的是( )
+Mn2++H2O(未配平)。下列说法正确的是( )
A.反应Ⅰ中Cu2S既是氧化剂又是还原剂
B.反应Ⅰ中每生成1mol![]() ,转移电子的物质的量为10mol
,转移电子的物质的量为10mol
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为1:3
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO4的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量之比为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某浓度的H2A溶液中滴加NaOH溶液,若定义pc=-lgc,则测得pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法错误的是( )
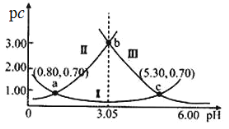
A.pH=3时溶液中c(A2-)>c(H2A)>c(HA-)
B.常温下,H2A的Ka1=10-0.80,Ka2=10-5.30
C.NaHA溶液中c(H+)>c(OH-)
D.从a点到c点,![]() 先增大后减小
先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于一定条件下的化学平衡H2(g)+I2(g)![]() 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
A.恒温恒容,充入H2,v(正)增大,平衡右移
B.恒温恒容,充入He,v(正)增大,平衡右移
C.加压,v(正),v(逆)不变,平衡不移动
D.升温,v(正)减小,v(逆)增大,平衡左移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:气体A的饱和溶液![]() A和食盐的饱和溶液
A和食盐的饱和溶液![]() 悬浊液
悬浊液![]() 晶体
晶体![]() 纯碱,则下列叙述错误的是( )
纯碱,则下列叙述错误的是( )
A.A气体是CO2,B气体是NH3
B.第Ⅲ步得到的晶体是发酵粉的主要成分
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作不正确的是( )
A.酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液
C.滴定时,眼睛观察锥形瓶中溶液颜色的变化
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S存在于多种燃气中,脱除燃气中H2S的方法很多。
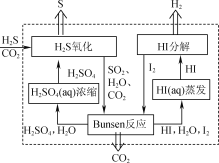
(1) 2019年3月《science direct》介绍的化学链技术脱除H2S的原理如图所示。
①“H2S氧化”反应中氧化剂与还原剂的物质的量之比为________。
②“HI分解”时,每1 mol HI分解生成碘蒸气和氢气时,吸收13 kJ的热量,写出该反应的热化学方程式:________。
③“Bunsen反应”的离子方程式为________。
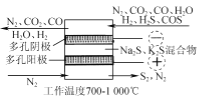
(2) 电化学干法氧化法脱除H2S的原理如图所示。阳极发生的电极反应为________;阴极上COS发生的电极反应为________。
(3) 用Fe2(SO4)3吸收液脱除H2S法包含的反应如下:
(Ⅰ) H2S(g)![]() H2S(aq)
H2S(aq)
(Ⅱ) H2S(aq) ![]() H++HS-
H++HS-
(Ⅲ) HS-+2Fe3+=S↓+2Fe2++H+
一定条件下测得脱硫率与Fe3+浓度的关系如图所示。

①吸收液经过滤出S后,滤液需进行再生,较经济的再生方法是________。
②图中当Fe3+的浓度大于10 g·L-1时,浓度越大,脱硫率越低,这是由于________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com