
【题目】请回答下列问题。
(1)碳酸氢钠俗称小苏打,其水溶液显____________性(填“酸”、“碱”或“中”) ;
(2)等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者____________后者(填“>”、“<”或“=”) ;
(3)除去碳酸钠固体中碳酸氢钠的方法是____________(填“加热”或“溶解过滤”) ;
(4)若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________;
(5)将一小块金属钠投入水中,发生反应的离子方程式为_________________________;
(6)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化。请写出此反应的化学方程式________________。
【答案】 碱 = 加热 Na2CO3 2Na + 2H2O =2 Na+ + 2OH- + H2↑ 4Al +3 O2 = 2Al2O3
【解析】(1)碳酸氢钠属于弱酸强碱盐,在水溶液中HCO3-既能发生水解反应(HCO3-+H2O![]() H2CO3+OH-),又能发生电离(HCO3-
H2CO3+OH-),又能发生电离(HCO3-![]() CO32-+H+),但水解程度大于电离程度,导致c(OH-)> c(H+),所以其水溶液呈碱性。
CO32-+H+),但水解程度大于电离程度,导致c(OH-)> c(H+),所以其水溶液呈碱性。
(2)等物质的量的碳酸钠和碳酸氢钠里碳元素的物质的量相等,根据碳元素守恒,它们与足量的盐酸反应离子方程式分别为Na2CO3+2HCl![]() 2NaCl+CO2↑+H2O和 NaHCO3+HCl
2NaCl+CO2↑+H2O和 NaHCO3+HCl![]() NaCl+CO2↑+H2O,所以产生的CO2的量也相等。
NaCl+CO2↑+H2O,所以产生的CO2的量也相等。
(3)由于碳酸钠比碳酸氢钠稳定,所以可通过加热使碳酸氢钠分解的方法除去碳酸钠固体中的碳酸氢钠。
(4)根据钠的性质推知其在潮湿空气中的一系列变化为: Na![]() Na2O
Na2O![]() NaOH
NaOH![]() Na2CO3·10H2O
Na2CO3·10H2O![]() Na2CO3,所以金属钠长时间在潮湿的空气中放置,最后生成的物质是碳酸钠。
Na2CO3,所以金属钠长时间在潮湿的空气中放置,最后生成的物质是碳酸钠。
(5)金属钠与水反应的离子方程式为2Na+2H2O![]() 2Na++2OH-+H2↑
2Na++2OH-+H2↑
(6) 比较活泼的金属铝,极易被空气中的氧气氧化而生成致密的氧化铝膜,从而保护内部的铝不再被氧化,反应的化学方程式为4Al +3 O2 = 2Al2O3。


科目:高中化学 来源: 题型:
【题目】乙二醇(沸点:197.3℃)是一种重要的的基础化工原料。由煤基合成气(主要成分CO、H2)与氧气先制备得到草酸二甲酯(沸点:164.5℃),再加氢间接合成乙二醇,具有反应条件温和、环境污染小等优点。反应过程如下:
反应 I:4NO(g)+ 4CH3OH (g)+ O2 (g)![]() 4CH3ONO(g)+ 2H2O(g) △H1=a kJ·mol-1
4CH3ONO(g)+ 2H2O(g) △H1=a kJ·mol-1
反应 II:2CO(g)+2CH3ONO(g)![]() CH3OOCCOOCH3(l)+2NO(g) △H2=bkJ·mol-1
CH3OOCCOOCH3(l)+2NO(g) △H2=bkJ·mol-1
反应III:CH3OOCCOOCH3 (1)+ 4H2(g)![]() HOCH2CH2OH(1)+ 2CH3OH (g) △H3=ckJ·mol-1
HOCH2CH2OH(1)+ 2CH3OH (g) △H3=ckJ·mol-1
(1)煤基合成气间接合成乙二醇的总热化学方程式是_________,在较低温条件下,该反应能自发进行的可能原因是_________。
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2L的密闭容器中发生反应II,达到平衡时NO的体积分数33.3%,若此时向容器中通入0.4molNO,一段时间后,重新达到新平衡时NO的体积分数_________33.3% (填“>”、“=”、“<”)。
(3)温度改变对反应II的催化剂活性有影响,评价催化剂活性参数:空时收率和CO选择性,表示式如下:
空时收率=![]()
CO的选择性=![]() ×100%
×100%
在不同温度下,某兴趣小组对四组其他条件都相同的反应物进行研究,经过相同时间t小时,测得空时收率、CO选择性数据如下表所示。
反应温度(℃) | 空时收率(g· mL-1· h-1) | CO的选择性(% ) |
130 | 0.70 | ① 72.5 |
140 | 0.75 | ② 71.0 |
150 | 0.71 | ③ 55.6 |
160 | 0.66 | ④ 63.3 |
下列说法正确的是_________。
A.温度升高,空时收率先增大后减少,说明△H2>0
B.温度升高,催化剂活性逐渐减弱,对CO的选择性逐渐降低,所以数据④肯定错误
C.130℃时,CO的选择性最高,说明CO生成CH3OOCCOOCH3的转化率最高
D.综合考虑空时收率和CO的选择性,工业生成CH3OOCCOOCH3时,选择140℃效果最好
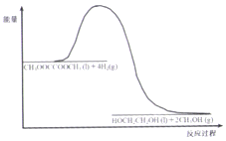
(4)120℃、常压时,CH3OOCCOOCH3+4H2![]() HOCH2CH2OH +2CH3OH 反应过程中能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中能量变化图。_______
HOCH2CH2OH +2CH3OH 反应过程中能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中能量变化图。_______
(5)研究证实,乙二醇、氧气可以在碱性溶液中形成燃料电池,负极的电极反应式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36 号元素),对 比中学常见元素周期表思考扇形元素周期表的 填充规律,并用化学用语.回答下列问题:
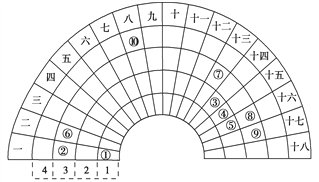
(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是____________
(2)比较元素最高价氧化物对应水化物的碱性:②_____________⑥(填“>”或“<”)
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:___________,设计一个简单的实验检验其阳离子的存在:___________________。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________。
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将CO2气体缓缓地通入到含2 mol KOH、1 mol Ba(OH)2和2 mol KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是

A.A~B段和C~D段发生的反应相同
B.B~C段反应的离子方程式是A1O2-+2H2O+CO2=Al(OH)3↓+HCO3-
C.V=134.4 L,n=3mol
D.D点所得溶液中离子浓度的关系为:c(K+)>c(CO32-)>c(OH﹣)>c(HCO3-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中![]() 的含量变化来监测核电站是否发生放射性物质泄漏。下列有关
的含量变化来监测核电站是否发生放射性物质泄漏。下列有关![]() 的叙述中错误的是
的叙述中错误的是
A. ![]() 的化学性质与
的化学性质与![]() 相同 B.
相同 B. ![]() 的原子序数为53
的原子序数为53
C. ![]() 的原子核外电子数为78 D.
的原子核外电子数为78 D. ![]() 的原子核内中子数多于质子数
的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在稀溶液中,强酸跟强碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)该图中有两处未画出,它们是______________、________________。
(2)做一次完整的中和热测定实验,温度计需使用________次。
(3)把温度为15.0 ℃,浓度为0.5 mol·L-1的酸溶液和0.55 mol·L-1的碱溶液各50 mL混合(溶液密度均为1 g·mL-1),生成溶液的比热容c=4.18 J · g-1 · ℃-1,轻轻搅动,测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热 |
HCl+NaOH | 15.0 | 18.4 | ΔH1 |
HCl+NH3·H2O | 15.0 | 18.1 | ΔH2 |
①计算上述第一组实验测出的中和热ΔH1=______。
②写出HCl+NH3·H2O的热化学方程式:____________________________________。
③两组实验结果差异的原因是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO![]() +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
MnO![]() +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-
MnO![]() +e-===MnO
+e-===MnO![]() (溶液呈绿色)
(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的_______影响。
(2)将SO2通入高锰酸钾溶液中,发生氧化还原反应的离子方程式为______________。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________(填字母)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com