
| A. | Fe→FeSO4 | B. | Cu(NO3)2→Cu | C. | CO→CO2 | D. | NaCl→AgCl |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉有大量氢气产生的溶液中:Ca2+、K+、NO3-、C1- | |
| B. | PH=0的无色溶液中:Na+、K+、MnO4-、NO3- | |
| C. | 在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+ | |
| D. | 在c(OH-)=1×10-13的溶液中:NH4+、Ca2+、C1-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| B. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| C. | CH3CH=CH2+Br2→CH3CHBrCH2Br | |
| D. | CHCl3+HF→CHFCl2+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 431kJ/mol | B. | 946 kJ/mol | C. | 649 kJ/mol | D. | 869 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al(OH)3(s)+NaOH(aq)═NaAlO2(aq)+2H2O(aq)△H<0 | |
| B. | CH3CH3OH(l)+3O2(g)-→2CO2(g)+3H2O(l)△H<0 | |
| C. | CO2(g)+C(g)═2CO(g)△H>0 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加A的量,化学平衡向右移动 | |
| B. | 温度升高,化学平衡一定会发生移动 | |
| C. | 增大压强,缩小容器体积,化学平衡不移动 | |
| D. | 添加MnO2,化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
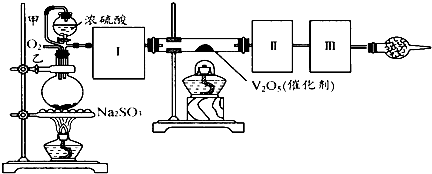

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
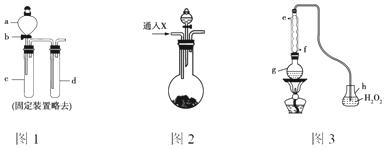
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com