
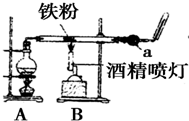
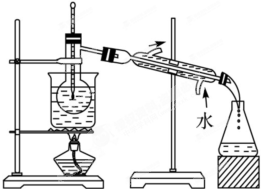
 如图是铁与水蒸气反应的实验装置.某同学在硬质玻璃管中放入足量还原性铁粉和少量石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,进行高温下铁与水蒸气反应的实验.请回答下列问题:
如图是铁与水蒸气反应的实验装置.某同学在硬质玻璃管中放入足量还原性铁粉和少量石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,进行高温下铁与水蒸气反应的实验.请回答下列问题:| 操作 | 现象 | 结论 | 解释(用离子方 程式表示) |
| 将反应后的固体全部取出置于烧杯中,加入足量的盐酸,溶解后过滤,立即向滤液中滴加KSCN溶液,观察溶液的颜色. | 滴加KSCN溶液后,溶液不变红色 | ① ② |
| ||
| ||


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
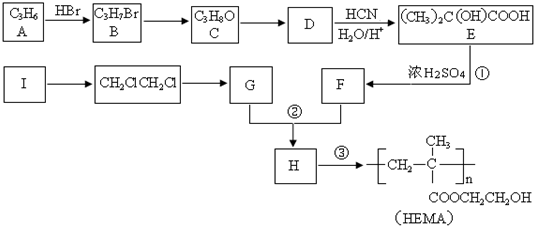
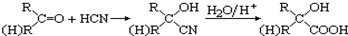
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发操作时,应使蒸发皿中的水分完全离干后,才能停止加热 |
| B、加入盐酸,放出无色气体,该气体能使澄清石灰水变浑浊的气体,则原溶液中有CO32- |
| C、除去铜粉中混有的少量镁粉和铝粉可加入足够稀盐酸,反应后过滤、洗涤 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
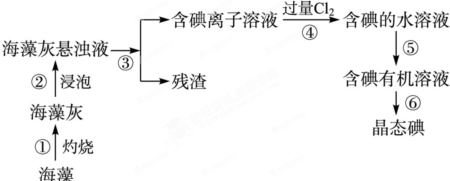
查看答案和解析>>
科目:高中化学 来源: 题型:
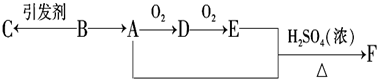
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,pH=12的1.0L NaClO溶液中水电离出的OH-的数目为0.01NA |
| B、等物质的量的N2和C0所含电子数均为NA |
| C、Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| D、在c(H+)水?c(OH-)水=10-26的溶液中能大量共存:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
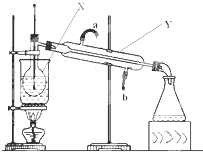 用NaOH固体配制100mL2.0mol/L NaOH溶液,其操作可以分为以下几步(容量瓶已检查完好,瓶口处不漏水):
用NaOH固体配制100mL2.0mol/L NaOH溶液,其操作可以分为以下几步(容量瓶已检查完好,瓶口处不漏水):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com