
| A. | 10 | B. | 18 | C. | 26 | D. | 30 |
分析 一至七周期中含有的元素种类数分别为:2、8、8、18、18、32、26种元素,以此来解答.
解答 解:因周期表中1~6周期所含元素种数为2、8、8、18、18、32,第7周期未排满,
而相邻周期同一主族元素原子序数之差,若元素为ⅠA、ⅡA族元素,则等于上一周期元素的种类,
若为其他主族元素等于下一周期元素的种类,
因此,同一主族相邻元素核外电子数(或原子序数)可能相差2、8、18或32,
若不相邻,那么它们相差的电子数可能为2+8=10、8+18=26等,不可能相差30,
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握每个周期元素的种类数、元素的位置为解答的关键,侧重分析与应用能力的考查,注意元素种类数的组合,题目难度不大.


 同步轻松练习系列答案
同步轻松练习系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.160 | 0.143 | 0.075 | 0.074 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 元素的非金属性:Z>W | |
| B. | 最高价氧化物对应水化物的碱性:X>Y | |
| C. | 离子半径:W2->Z3->X2+>Y3+ | |
| D. | 气态氢化物的稳定性:Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:C>D>A>B | B. | 离子半径:D>C>A>B | ||
| C. | 原子序数:B>A>D>C | D. | 氢化物稳定性:D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有20 种元素 | |
| C. | 科学研究时,经常在金属、非金属分界处寻找半导体材料 | |
| D. | 元素周期表共七个横行代表七个周期,18 个纵列代表18 个族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出热量如图所示.
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出热量如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al | |
| B. | 可以用钠加入氯化镁饱和溶液中制取镁 | |
| C. | 炼铁高炉中所发生的反应都是放热的,故无需加热 | |
| D. | 金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
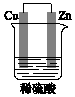 某原电池装置如图所示.
某原电池装置如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com