
如图由锌—铜—稀H2SO4组成的原电池装置中,当导线中有0.2 mol电子通过时,理论上两极的变化是( )

A.铜片增重6.4g B.锌片增重6.5 g
C.铜片上析出0.1 mol O2 D.锌片溶解了6.5 g
科目:高中化学 来源:2014-2015学年辽宁大连市高二上期中考试化学试卷(解析版) 题型:填空题
(10分)已知水在25℃和95℃时,其电离平衡曲线如下图所示:
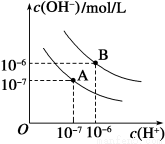
(1)则25℃时水的电离平衡曲线应为 (填“A”或“B”)。
(2)95℃时水的离子积KW= 。
(3)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 。
(4)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
(5)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析其原因: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁大连市高一上期中考试化学试卷(解析版) 题型:选择题
进行实验必须注意安全,下列说法正确的是
A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B.不慎将浓碱溶液沾到皮肤上,要立即用盐酸冲洗
C.用点燃的火柴在液化气钢瓶口检验是否漏气
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省高二上学期半期考试化学试卷(解析版) 题型:选择题
用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是 ( )
A. 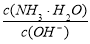 B.
B. 
C.c(H+)和c(OH-)的乘积 D.OH-的物质的量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第一次月考化学试卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu,则下列说法正确的是

A.电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ
B.电极Ⅰ发生还原反应
C.电极Ⅳ逐渐溶解
D.电极Ⅲ的电极反应:Cu-2e-===Cu2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第一次月考化学试卷(解析版) 题型:选择题
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做( )
A.正极 B.负极 C.阴极 D.阳极
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第一次月考化学试卷(解析版) 题型:填空题
(11分)某化学兴趣小组拟用下图装置测定某粗锌样品中锌的质量分数。他们查阅资料后获知该粗锌样品中的其他成分不能与稀盐酸反应。请填写以下实验报告。
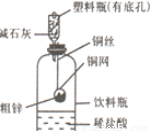
(1)实验目的: ;
(2)实验步骤:
①称取10.0 g粗锌置于铜网中,按图示装置组装后,称得仪器和药品总质量为120.0 g。
②将铜网插入足量的稀盐酸中,有关反应的化学方程式为 ;
③反应完全后,称得装置总质量为119.8 g,则粗锌中锌的质量分数为 ;
(3)问题探究:(已知碱石灰是NaOH和CaO的混合物,常用于干燥、吸收气体。)
①该实验若不用碱石灰,则所测得的粗锌中锌的质量分数将 ;(填“偏大”、“偏小”或“无影响”)。
②若将粗锌换成某含有杂质的石灰石样品(杂质也不与稀盐酸反应),判断该实验方案能不能用于石灰石样品中CaCO3质量分数的测定,并说明理由。
。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第一次月考化学试卷(解析版) 题型:选择题
分类是学习和研究化学的一种重要方法,下列分类合理的是
A.K2CO3和K2O都属于盐B.H2SO4和HNO3都属于酸
C.KOH和Na2CO3都属于碱 D.Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高一9月月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列叙述中正确的是( )
①106 g Na2CO3晶体中的离子总数大于3NA
②标准状况下,16 gO3和O2混合气体中含有的氧原子数为NA
③将0.1mol NaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1NA
④1 mo1 N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
A.①② B.②④ C.①③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com