
【题目】如图所示,A为电源,B为浸透饱和食盐水和酚酞的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1 ,断开K2 ,通电后,d端显红色,则电源a端为______极,若c、d为惰性电极,c端的电极反应是____________________________________
检验c端产物的方法_______________________________________________
高锰酸钾液滴现象__________________________________________________
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3 ,且均为0.1 mol,断开K1,闭合K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+ 氧化能力由大到小的顺序是_______;

(3)D装置中反应的方程式 ___________________________
【答案】正 2Cl--2e-=Cl2↑ 将湿润的淀粉碘化钾试纸置于电极附近,试纸变蓝 紫红色向c极移动 Cu2+>H+>X3+; Cu+H2SO4![]() CuSO4+H2↑
CuSO4+H2↑
【解析】
(1)关闭K1,打开K2,为电解饱和食盐水装置,其电解总反应为:2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑,d端呈红色,说明d端生成了OH-,由此可知,b为电源负极,a端为电源正极;c为电解池的阳极,若c为惰性电极,其电极反应式为:2Cl--2e-=Cl2↑;c端产物为Cl2,常用湿润淀粉碘化钾试纸检验,其检验方法为:将湿润的淀粉碘化钾试纸置于电极附近,若试纸变蓝,则说明生成了Cl2;KMnO4溶液为电解质溶液,电解过程中,c端Cl-被氧化,MnO4-向c极移动,其现象为:紫红色向c极移动;
2OH-+Cl2↑+H2↑,d端呈红色,说明d端生成了OH-,由此可知,b为电源负极,a端为电源正极;c为电解池的阳极,若c为惰性电极,其电极反应式为:2Cl--2e-=Cl2↑;c端产物为Cl2,常用湿润淀粉碘化钾试纸检验,其检验方法为:将湿润的淀粉碘化钾试纸置于电极附近,若试纸变蓝,则说明生成了Cl2;KMnO4溶液为电解质溶液,电解过程中,c端Cl-被氧化,MnO4-向c极移动,其现象为:紫红色向c极移动;
(2)根据电解C的图象可知,通电后就有固体生成,当通过电子为0.2mol时,析出固体质量达最大,证明此时析出的固体是铜。如果是X3+析出,电子数应该是0.3mol,则氧化能力为Cu2+>X3+,当电子超过0.2mol时,固体质量没变,说明这是阴极产生的是氢气,即电解水,说明氧化能力H+>X3+,故氧化能力为Cu2+>H+>X3+;
(3)断开K1,闭合K2,由(1)分析已知b为电源负极,即D装置中碳棒作为阴极,Cu电极作为阳极,阴极上的电极反应是H+得到电子,阳极上是Cu失去电子,故D装置中反应的化学方程式为:Cu+H2SO4![]() CuSO4+H2↑。
CuSO4+H2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】亚磷酸二乙酯[HPO(OC2H5)2]是一种液态阻燃增塑剂。实验室采用PCl3和无水乙醇制备高纯度亚磷酸二乙酯,反应方程式为:PCl3 + 4C2H5OH → HPO(OC2H5)2 + HCl↑+2C2H5Cl + H2O;实验步骤如下:

①将45 mL CHCl3和46.00 g(1.0 mol)无水乙醇混合后加入250 mL三颈烧瓶中。
②从仪器A中滴加20 mL CHCl3和41.25 g (0.3 mol)PCl3混合溶液,用冰水控温6~8℃,开动搅拌器,约1 h滴加完毕。
③将反应物倒入烧杯中,用10%的Na2CO3溶液调节pH至7~8,再用去离子水洗涤三次,在仪器B中分离。
④减压蒸馏,收集产品,得29.60 g产品。
(1)装置图中仪器A为恒压滴液漏斗,其中支管的作用为______;倒置漏斗的作用为______;步骤③中仪器B名称为______。
(2)用碳酸钠溶液洗涤的目的是为了除去酸性物质______(填化学式)以及PCl3;
(3)从无水乙醇利用角度计算,本次实验产率为______(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应mA(g)+nB(s)![]() 3C(g)达到平衡时,测得c(A)为0.5 mol/L。在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.3 mol/L,则下列判断不正确的是
3C(g)达到平衡时,测得c(A)为0.5 mol/L。在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.3 mol/L,则下列判断不正确的是
A.混合气体密度一定减小B.平衡一定向逆反应方向移动
C.化学计量数:m+n>3D.物质C的体积分数增加了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的 NO(g)和足量C(s),发生反应 C(s)+2NO(g)![]() CO2(g)+N2(g),平衡状态时 NO(g)的物质的量浓度 c(NO)与温度 T 的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时 NO(g)的物质的量浓度 c(NO)与温度 T 的关系如图所示。则下列说法中正确的是( )

A.该反应的 ΔH>0B.若该反应在 T1、T2 时的平衡常数分别为 K1、K2,则 K1<K2
C.在 T3 时,若混合气体的密度不再变化,则可以判断反应达到平衡状态 CD.在 T2 时,若反应体系处于状态D,则此时一定有 v 正<v 逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烯烃为原料,合成某些高聚物的路线如下:
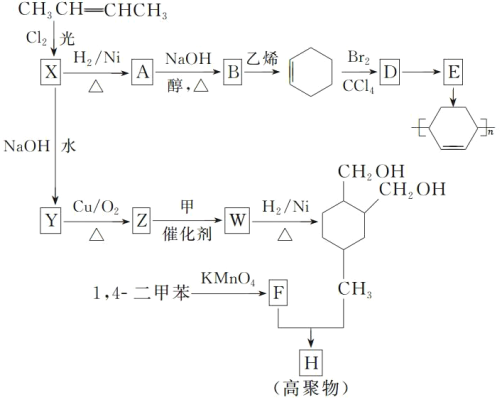
已知:

(1)CH3CH=CHCH3 的名称是_____。
(2)X 中含有的官能团是_____。
(3)A→B 的化学方程式是_____。
(4)D→E 的反应类型是_____。
(5)甲为烃,F 能与 NaHCO3 反应产生 CO2。
①下列有关说法正确的是_____。
a.有机物Z 能发生银镜反应
b.有机物Y 与HOCH2CH2OH 互为同系物
c.有机物Y 的沸点比 B 低
d.有机物F 能与己二胺缩聚成聚合物
②Y 的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的结构简式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是
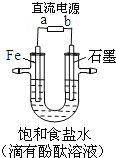
A.a 为电源的正极
B.通电一段时间后,石墨电极附近溶液先变红
C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑
D.电解饱和食盐水的总反应是:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的有( )
①用电子式表示HCl的形成过程:![]()
②MgCl2的电子式:![]() ③质量数为133、中子数为78的铯原子:
③质量数为133、中子数为78的铯原子:![]() Cs
Cs
④乙烯、乙醇结构简式依次为:CH2=CH2、C2H6O ⑤S2﹣的结构示意图:![]()
⑥次氯酸分子的结构式:H-O-Cl ⑦CO2的分子模型示意图:![]()
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
A.均减半B.均加倍C.均增加1molD.均减少1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃,分别向10ml浓度均为1mol/L的两种弱酸HA、HB中不断加水稀释,并用pH传感器测定溶液pH。所得溶液pH的两倍(2pH)与溶液浓度的对数(1gc)的关系如图所示。下列叙述正确的是
己知:(1)HA的电离平衡常数Ka=[c(H+)·c(A-)]/[c(HA)-c(A-)]≈c2(H+)/c(HA);(2)pKa=-lgKa

A. 弱酸的Ka随溶液浓度的降低而增大
B. a点对应的溶液中c(HA)=0.1mol/L,pH=4
C. 酸性:HA<HB
D. 弱酸HB的pKa=5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com