
| A、实验室中用稀盐酸与石灰石反应制取CO2 |
| B、实验室中用高锰酸钾加热分解制取O2 |
| C、实验室中用浓盐酸与二氧化锰加热制取Cl2 |
| D、实验室中用稀硫酸与锌粒反应制取H2 |


科目:高中化学 来源: 题型:
| A、Cl-、NH4+、Na+、K+ |
| B、Fe3+、CH3COO-、K+、Ba2+ |
| C、CO32-、SO42-、Cl-、Na+ |
| D、NH4+、Mg2+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
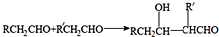
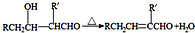
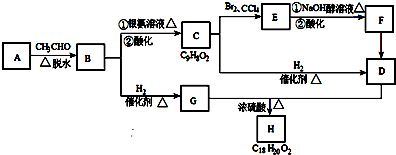
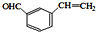
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、多肽、油脂、纤维素、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应 |
| B、福尔马林、葡萄糖溶液与新制氢氧化铜悬浊液共热,都会有砖红色沉淀产生 |
| C、棉、麻、蚕丝、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| D、根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+2H2O═2NaOH+H2↑ | ||||
B、C+H2O(g)
| ||||
| C、CaO+H2O═Ca(OH)2 | ||||
| D、Cl2+H2O═HCl+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 | 结论 | |
| A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显橙红色 | 原溶液中有Br- |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| D | 滴加稀盐酸,产生无色无味气体,将气体通入澄清石灰水中 | 生成白色沉淀 | 原溶液中有CO32- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol?L-1 H2C2O4溶液 | 30mL 0.01mol?L-1 KMnO4溶液 |
| ② | 20mL 0.2mol?L-1 H2C2O4溶液 | 30mL 0.01mol?L-1 KMnO4溶液 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com