
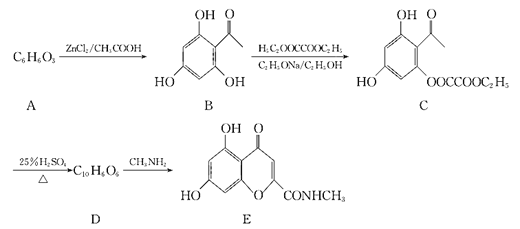
����Ŀ�����ͪ�������ɱ�淽���ر�Զ����нϺõ�ɱ�����ã��ҹ���ѧ���о���һ�����ͪ�����ĺϳ�·�����£�
�ش��������⣺
(1)A�Ļ�ѧ����Ϊ_________
(2)B�к��������ŵ�������__________
(3)B��C�ķ�Ӧ������_____________
(4)д��C����������������Һ��Ӧ�Ļ�ѧ����ʽ��____________
(5)D�Ľṹ��ʽΪ__________��
(6)д����B��Ϊͬ���칹�����ʹFe3+��ɫ����1mol�û���������������4molNaOH�Ļ�����Ľṹ��ʽ(�˴Ź�������Ϊ����壬�������Ϊ1��2��2��3)��_________��
(7)������ɱ��Ӻ������Ϊ��ʼԭ���Ʊ�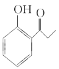 �ĺϳ�·��___________ (���Լ���ѡ)��
�ĺϳ�·��___________ (���Լ���ѡ)��
���𰸡��������ӻ�1��3��5������ �ǻ����ʻ� ȡ����Ӧ 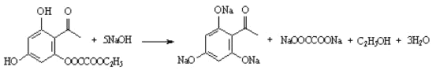

 ��
��![]() ��
�� 
��������
A����ȡ����Ӧ����B������B�ṹ��ʽ��A����ʽ֪��AΪ ��B����ȡ����Ӧ����C��D����ȡ����Ӧ����E������E�ṹ��ʽ��D����ʽ֪��DΪ
��B����ȡ����Ӧ����C��D����ȡ����Ӧ����E������E�ṹ��ʽ��D����ʽ֪��DΪ ��
��
��1��AΪ ��A�Ļ�ѧ����Ϊ�������ӻ�1��3��5�����ӣ��ʴ�Ϊ���������ӻ�1��3��5�����ӣ�
��A�Ļ�ѧ����Ϊ�������ӻ�1��3��5�����ӣ��ʴ�Ϊ���������ӻ�1��3��5�����ӣ�
��2��B�к��������ŵ��������ǻ����ʻ����ʴ�Ϊ���ǻ����ʻ���
��3��B��C�ķ�Ӧ������ȡ����Ӧ���ʴ�Ϊ��ȡ����Ӧ��
��4��C����������������Һ��Ӧ�Ļ�ѧ����ʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��D�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��6����B��Ϊͬ���칹�����ʹFe3+��ɫ��˵�����з��ǻ����ܷ���ˮ�ⷴӦ��˵�������������˴Ź�������Ϊ����壬�������Ϊ1:2:2:3�����������Ľṹ��ʽΪ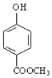 ��
��![]() ��
��
�ʴ�Ϊ�� ��
��![]() ��
��
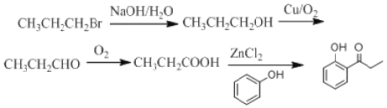
��7���ɱ��Ӻ������Ϊ��ʼԭ���Ʊ�![]() ��1����鷢��ȡ����Ӧ����1������1����������������Ӧ���ɱ�ȩ����ȩ����������Ӧ���ɱ��ᣬ����ͱ��ӷ���ȡ����Ӧ����
��1����鷢��ȡ����Ӧ����1������1����������������Ӧ���ɱ�ȩ����ȩ����������Ӧ���ɱ��ᣬ����ͱ��ӷ���ȡ����Ӧ����![]() ����ϳ�·��Ϊ��
����ϳ�·��Ϊ�� ��
��
�ʴ�Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��NaOH��Һ���ζ��ڱ������������Һ�����в�����
������Һ�м���1��2��ָʾ��
��ȡ20.00 mL����Һ������ƿ��
����NaOH��Һ�ζ����յ㣨�յ�ʱ��Һ��pHԼΪ9.1��
���ظ����ϲ���
������ƽ��ȷ��ȡһ�������ڱ���������ع������250 mL����Һ�����pHԼΪ4.2��
����ʵ�����ݼ���NaOH�����ʵ���Ũ��
��1�����ϸ����У���ȷ�ģ�����ţ�����˳����_____________________________����������ʹ�õ���������ƿ�⣬����Ҫʹ�õ�������______________��
��2��ѡ��ָʾ����______________���ζ��յ�����______________________________________��
��3���ζ�������¼NaOH���ն������ظ��ζ����Σ����ݼ�¼���±���
�ζ�����ʵ������ | 1 | 2 | 3 | 4 |
V����Ʒ��/mL | 20.00 | 20.00 | 20.00 | 20.00 |
V��NaOH��/mL���������� | 0.10 | 0.30 | 0.00 | 0.20 |
V��NaOH��/mL���ն����� | 20.08 | 20.30 | 20.80 | 20.22 |
V��NaOH��/mL�����ģ� | 19.98 | 20.00 | 20.80 | 20.02 |
ijͬѧ�ڴ������ݹ����м���õ�ƽ������NaOH��Һ�����ΪV��NaOH������19.98+20.00+20.80+20.02��/4mL��20.20mL�����ļ��������������_______________��
��4����������ڹ۲�ζ��ܵ���ʼ����ʱ��Ҫʹ�ζ��ܵļ��첿�ֳ�����Һ���ζ�ǰ������ˮϴ����ʽ�ζ��ܣ�Ȼ���NaOH��Һ���еζ����˲�����ʵ����________������ƫ��������ƫС��������Ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ����������ʯī������ʢ�б���NaCl��Һ��U���С����з�����ȷ�ģ���

A. K1�պϣ������Ϸ����ķ�ӦΪ2H����2e��=H2��
B. K1�պϣ�ʯī����Χ��Һ������ǿ
C. K2�պϣ��������ᱻ��ʴ��������������������������
D. K2�պϣ���·��ͨ��0.002NA������ʱ������������0.001mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L������3�����ʼ���з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ����Ӧ��t1 minʱ����ƽ�⣬��ͼ��ʾ��

(1)�÷�Ӧ�Ļ�ѧ����ʽ��_________����t1=10min����X��ʾ��ѧ��Ӧ����Ϊ_________
(2)��������Ӧ��X��Y��Z�ֱ�ΪNH3��H2��N2�� ����֪1mol�����ֽ�ɵ���������Ҫ����46kJ������������t1 minʱ���÷�Ӧ���յ�����Ϊ_______��
(3)���������¶Ȳ��䣬��С�����������ѧ��Ӧ����_______(����������������С������������)����ѧƽ�ⳣ��K_______ (����������������С������������)
(4)��һ���ݻ����ܱ�������,�������»�ѧ��Ӧ��CO2(g)+H2(g)![]() CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���ʾ��
CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���ʾ��
t/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=__________
�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������_______
A.������ѹǿ���� B.���������c(CO)����
C.v��(H2)=v��(H2O) D.c(CO2)=c(CO)
(5)ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)=c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ__________�棻
(6)��800��ʱ������������Ӧ,ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)=2mol��L-1,c(H2)=1.5mol��L-1��c(CO)=1mol��L-1��c(H2O)=3mol��L-1������һʱ�̣���Ӧ��__________(��"����Ӧ"��"�淴Ӧ")������С�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������(CrO3)�轺���Բ�Ƽݡ�Ԫ��Cr�ļ��ֻ�����ת����ϵ��ͼ��ʾ�������ж���ȷ����
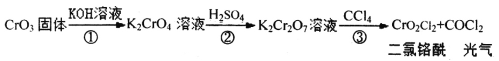
A.��Ӧ�ٱ���CrO3�����������������
B.CrO42-�ڼ�����Һ�в��ܴ�������
C.ֻ�з�Ӧ��Ϊ������ԭ��Ӧ
D.��̬��ԭ�ӵļ۵����Ų�ʽΪ3d44s2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��������٤������������˵����ȷ���ǣ� ��
A.��״���£�560mL�������������Ļ�������ַ�Ӧ�ۼ���ĿΪ0.05NA
B.��״���£�2.24LCl2ͨ��NaOH��Һ�з�Ӧת�Ƶĵ�����Ϊ0.2NA
C.���³�ѹ�£�1.5molHCHO��C2H2O3�Ļ������ȫ���ȼ�գ����ĵ�O2������ĿΪ1.5NA
D.0.1mol/L��NH4Cl��Һ��ͨ���������������ԣ���ʱ��Һ��NH4+��ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ���ͬ�������ܱ�����M��N���������¶�Ϊ150 ��,��M�����м���a mol HI��ͬʱ��N�����м���b mol HI (a>b)������Ӧ2HI(g)![]() H2 (g) + I2 (g) �ﵽƽ���������˵����ȷ����
H2 (g) + I2 (g) �ﵽƽ���������˵����ȷ����
A���ӷ�Ӧ��ʼ���ﵽƽ��,����ʱ��tM > tN
B��ƽ��ʱcM(I2) = c N(I2)
C��ƽ��ʱI2 �����ڻ�������е����������M > N
D��HI��ƽ��ֽ�����M = ��N
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2molCO��3molH2O�����2L���ܱ������У��������¿��淴Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g)��
CO2(g)+H2(g)��
��1���û�ѧ��Ӧ��ƽ�ⳣ������ʽ��___��
��2����֪��700��ʱ���÷�Ӧ��ƽ�ⳣ��K1=2������¶��·�ӦCO2��g��+H2��g��CO��g��+H2O��g����ƽ�ⳣ��K2=__����Ӧ2CO��g��+2H2O��g��2CO2��g��+2H2��g����ƽ�ⳣ��K3=___��
��3����֪��1000��ʱ���÷�Ӧ��ƽ�ⳣ��K4=1.0����÷�ӦΪ___��Ӧ������ȡ����ȡ�������H__0(�>����<��)��
��4����1000���£�ijʱ��CO2�����ʵ���Ϊ1mol�����ʱ��������__�����棩���>������=����<������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ���������ȡ��ȩ(�е�Ϊ20.8�棬����ˮ����)��װ��(�г�װ������)��ͼ��ʾ��

����˵���������
A.��Բ����ƿ�е���H2O2��Һǰ���K
B.ʵ�鿪ʼʱ���ȼ��Ȣڣ���ͨO2��Ȼ����Ȣ�
C.װ�â��з����ķ�ӦΪ2CH3CH2OH +O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.ʵ�����ʱ���Ƚ����еĵ����Ƴ�����ֹͣ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com