
【题目】下列图示与对应的叙述不相符合的是( ) 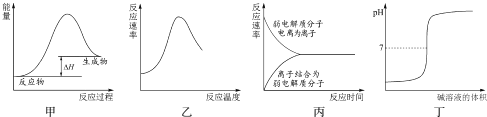
A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
【答案】A
【解析】A.燃料燃烧应放出热量,反应物总能量大于生成物总能量,而题目所给图为吸热反应,故A错误;
B.酶为蛋白质,温度过高,蛋白质变性,则酶催化能力降低,甚至失去催化活性,故B正确;
C.弱电解质存在电离平衡,平衡时正逆反应速率相等,图象符合电离特点,故C正确;
D.强碱滴定强酸,溶液pH增大,存在pH的突变,图象符合,故D正确.
故选A.
【考点精析】掌握弱电解质在水溶液中的电离平衡和酸碱中和滴定是解答本题的根本,需要知道当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理;中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:
【题目】氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.
下列说法错误的是( )
A.S2Cl2的结构式为Cl﹣S﹣S﹣Cl
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,分子间作用力:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知115号元素原子有七个电子层,且最外层有5个电子,试判断115号元素在元素周期表中的位置是( )
A. 第七周期第IIIA族B. 第七周期第VA族
C. 第五周期第VIIA族D. 第五周期第IIIA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2![]() SiCl4
SiCl4![]() Si
Si
B.FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C.N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3![]() MgCl2
MgCl2![]() Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂能增加食物的滋味,增进食欲,保证机体的正常生理功能.但摄入过量脂肪,可能引起肥胖、高血脂、高血压等.下列食品中富含油脂的是( )
A.苹果
B.大米
C.白菜
D.花生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种钠的化合物,W、X、Y、Z,它们之间存在如下关系:①W ![]() X+CO2+H2O;
X+CO2+H2O;
②Z+CO2→X+O2;
③Z+H2O→Y+O2↑;
④X+Ca(OH)2→Y+CaCO3↓.
问题:
(1)则X的俗名是 , Z中阴阳离子个数之比为
(2)写出反应③离子方程式:
(3)写出Ca(OH)2与过量W反应化学方程式:
(4)在体积和温度不变的密闭容器中,加入一定量的Z和一定量的CO2充分反应,测得反应前后压强之比为5:4,则反应后容器中CO2和O2物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是
( )
A.a点对应的溶液中:Na+、Fe3+、SO42﹣、HCO3﹣
B.b点对应的溶液中:Ag+、Ca2+、NO3﹣、F﹣
C.c点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
D.d点对应的溶液中:K+、NH4+、I﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学模拟工业制碘的方法,探究ClO3﹣和I﹣的反应规律.实验操作及现象如表:
实验及试剂 | 编号 | 无色NaClO3 | 试管中 | 淀粉KI |
| 1 | 0.05 mL | 浅黄色 | 无色 |
2 | 0.20 mL | 深黄色 | 无色 | |
3 | 0.25 mL | 浅黄色 | 蓝色 | |
4 | 0.30 mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如图实验: 
经检验,上述白色沉淀是AgCl.写出加入0.20mL NaClO3后,溶液中ClO3﹣和I﹣发生反应的离子方程式: .
(2)查阅资料:一定条件下,I﹣和I2都可以被氧化成IO3﹣ .
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)
中的反应产物继续反应,同时生成Cl2 .
进行实验:
①取少量实验4中的无色溶液进行如图实验,进一步佐证其中含有IO3﹣ . 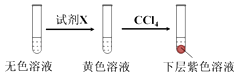
其中试剂X可以是(填字母序号).
a.碘水b.KMnO4溶液c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2 , 便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL 1.33molL﹣1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化.进行以上对比实验的目的是 , 进一步佐证实验4中生成了Cl2 . 获得结论:NaClO3溶液用量增加导致溶液褪色的原因是(用离子方程式表示).
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
编号 | 6.0 molL﹣1 H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
5 | 0.25 mL | 浅黄色 | 无色 |
6 | 0.85 mL | 无色 | 蓝色 |
①对比实验4和5,可以获得的结论是 .
②用离子方程式解释实验6的现象: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com