
【题目】最近科学家发现了氧元素的一种新的粒子O4。对于这种新粒子,下列说法不正确的是( )
A. 它与氧气互为同素异形体B. 它是氧元素的一种同位素
C. 它的摩尔质量是64 g·mol-1D. 它可能具有很强的氧化性
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应N2+3H22NH3 , △H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图1所示: 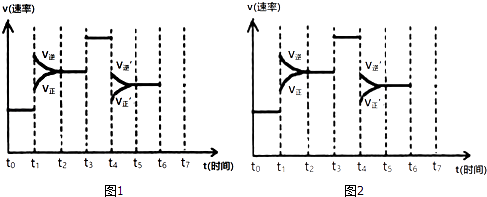
回答下列问题:
(1)处于平衡状态的时间段是(填选项).
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是:t1时刻;t3时刻;t4时刻 . (填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中结论,下列时间段中,氨的百分含量最高的是(填选项).
A.t0~t1
B.t2~t3
C.t3~t4
D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,若将密闭容器体积缩小一半,则对反应产生的影响是(填选项).
A.正反应速率减小,逆反应速率增大
B.正反应速率增大,逆反应速率减小
C.正、逆反应速率都减小
D.正、逆反应速率都增大
(5)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图2中画出反应速率的变化曲线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a克Fe2O3 、Al2O3 样品溶解在过量的200mL c(H+)=0.1molL﹣1 的硫酸溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+ 刚好完全沉淀,用去NaOH溶液100mL,则NaOH 溶液的浓度为( )
A.0.1 molL﹣1
B.0.2 molL﹣1
C.0.4 molL﹣1
D.0.8 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2Zn(OH)2ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2ZnCO3的工艺流程如图: 
请回答下列问题:
(1)当(NH4)2SO4 , NH3H2O的混合溶液中存在c(NH4+)=2c(SO42﹣)时,溶液呈(填“酸”、“碱”或“中”)性.
(2)“浸取”时为了提高锌的浸出率,可采取的措施是(任写一种).
(3)“浸取”时加入的NH3H2O过量,生成MnO2的离子方程式为 .
(4)适量S2﹣能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: . [已知:Ksp(ZnS)=1.6×10﹣24 , Ksp(CuS)=1.3×10﹣36]
(5)“沉锌”的离子方程式为 .
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知①N2+3H2 ![]() 2NH3;②3Cl2+8NH3=N2+6NH4Cl,判断下列物质的还原性从强到弱的顺序是( )
2NH3;②3Cl2+8NH3=N2+6NH4Cl,判断下列物质的还原性从强到弱的顺序是( )
A.NH4Cl>NH3>H2
B.H2>NH3>NH4Cl
C.NH3>NH4Cl>H2
D.H2>NH4Cl>NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com